BÁO CÁO THÍ NGHIẸM PHÂN TÍCH THỰC PHẨM 2 GIÁO VIÊN HƯỚNG DẪN ĐIỂM NHẬN XÉT CỦA GIÁO VIÊN 3 MỤC LỤC BÁO CÁO THÍ NGHIỆM SỐ 1 7 ĐỊNH LƯỢNG ĐỘ ẨM VÀ TRO BẰNG PHƯƠNG PHÁP TRỌNG LƯỢNG 7 1 Mục tiêu bài thí nghiệm 7 2 Nguyên tắc 7 3 Sơ đồ trình tự tiến hành thí nghiệm 8 4 Kết quả và xử lý số liệu 14 5 Bàn luận 16 6 Tài liệu tham khảo 20 BÁO CÁO THÍ NGHIỆM SỐ 2 21 ĐỊNH LƯỢNG NITƠ TỔNG BẰNG PHƯƠNG PHÁP KJELDAHL 21 1 Mục tiêu bài thí nghiệm 21 2 Nguyên tắc.
Mục tiêu bài thí nghiệm
• Định lượng hàm lượng tro
• Định lượng tổng rắn có trong mẫu lỏng
• Nắm được nguyên tắc và cách tiến hành định lượng của độ ẩm và hàm lượng tro của mẫu bằng phương pháp trọng lượng
Trong quá trình thí nghiệm, cần trình bày rõ nguyên tắc và trình tự tiến hành để đảm bảo tính chính xác Việc tính toán kết quả phải được thực hiện cẩn thận, đồng thời đánh giá kết quả thu được là rất quan trọng Các yếu tố ảnh hưởng đến kết quả thí nghiệm cũng cần được xác định và phân tích, bao gồm sai số có thể xảy ra trong quá trình thực hiện.
Nguyên tắc
Phương pháp xác định độ ẩm dựa trên sự giảm khối lượng của mẫu khi được làm nóng trong tú sấy Trong thí nghiệm, tủ sấy đối lưu được sử dụng ở nhiệt độ 105 °C để tách ẩm khỏi mẫu dạng bột hoặc chất lỏng Kết quả cho phép định lượng hàm lượng tro trong mẫu.
Phương pháp này dựa vào khối lượng tro trắng của mẫu sau khi tro hóa ở nhiệt độ và thời gian xác định Nếu tro có màu đen, cần để nguội, thêm vài giọt H2O2 hoặc HNO3 đậm đặc, sau đó nung lại cho đến khi đạt được tro trắng.
Sơ đồ trình tự tiến hành thí nghiệm
Vật liệu, dụng cụ và thiết bị
Hình 1.1 Mẫu bột bắp và sữa tươi Dụng cụ
• Lò nung điều chỉnh đượcc nhiệt độ
• Găng tay chịu nhiệt hoặc kẹp tay dài
• Cân phân tích 4 số lẻ
Hình 1.3 Tủ sấy trong phòng thí nghiệm
Cân đĩa peptri cùng với nắp
Cho 3g bột vào đĩa peptri
Lấy ra, để nguội Cân (cả đĩa và nắp)
Sấy (105 o C, 3 giờ) Lấy ra, để nguội
Cân đĩa peptri cùng mẫu vầ nắp
Sấy đĩa peptri (cả nắp)
• Cần đánh số và ghi thông tin cần thiết lên các vật chứa mẫu trong tủ sấy
• Sử dụng găng tay hoặc kẹp dài tay khi lấy các vật chứa từ tủ sấy
Trước khi tiến hành cân mẫu sau khi sấy, cần làm nguội cả mẫu và vật chứa trong bình hút ẩm Chỉ nên lấy chúng ra khỏi bình ngay trước khi thực hiện việc cân để đảm bảo độ chính xác.
• Mở bình hút ẩm bằng thao tác đẩy nắp sang ngang chứ không được kéo nắp lên trên
3.1 Xác định độ ẩm của mẫu bột bắp v Sơ đồ
Sơ đồ 1.1 Quy trình xác định độ ẩm của mẫu bột bắp v Giải thích quy trình
Để loại bỏ độ ẩm và giảm sai số khi tính phần trăm ẩm của mẫu, hãy sấy khô đĩa petri cùng nắp trong tủ sấy ở nhiệt độ 105°C trong 30 phút Đừng quên ghi số thứ tự lên cả đĩa và nắp.
Để đảm bảo độ chính xác khi cân đĩa và nắp, cần để nguội đĩa trong bình hút ẩm đến nhiệt độ phòng trước khi cân Việc cân khi đĩa chưa nguội hoàn toàn sẽ dẫn đến khối lượng không ổn định do sự thay đổi thể tích và khối lượng riêng theo nhiệt độ Hơn nữa, trong quá trình sấy đĩa petri, nước bốc hơi và có thể còn hơi nước xung quanh đĩa khi lấy ra, do đó việc làm nguội trong bình hút ẩm là cần thiết.
Để tiến hành thí nghiệm, hãy đặt khoảng 3 gram mẫu bột lên đĩa và cân chính xác cùng với nắp Sau đó, đặt đĩa chứa mẫu vào tủ sấy ở nhiệt độ 105 độ C trong 3 giờ Lưu ý không đậy nắp mà chỉ để bên cạnh hoặc kê hờ lên đĩa để không cản trở quá trình bốc hơi nước.
• Lấy đĩa ra khỏi tủ sấy, đậy nắp và để nguội trong bình hút ẩm, sau đó lấy ra cân
• Tính độ ẩm theo phần trăm khối lượng
3.2 Định lượng tổng chất rắn trong mẫu sữa lỏng (AOAC 990.19, 990.20) v Sơ đồ
Sơ đồ 1.2 Quy trình định lượng tổng rắn có trong mẫu sữa lỏng v Giải thích quy trình
• Ghi dấu và cân chính xác khối lượng chén nung đã được sấy khô từ trước
• Cho 5 g mẫu sữa vào chén và cân chính xác
Để làm bay hơi nước hiệu quả, hãy đun nóng chén trên bếp thay vì cho trực tiếp vào tủ sấy, vì phương pháp này tiết kiệm thời gian hơn Cần chú ý không làm mẫu bị khô hoàn toàn; hãy đun với lửa vừa phải và lắc nhẹ chén để sữa liên tục tiếp xúc với thành chén cho đến khi phần lớn nước được bay hơi.
Lấy ra, để nguội Cho 5g sữa vào chén
Sấy (105 o C, 3 giờ) Cân Đun nóng Chén nung (đã được sấy khô)
Vài gọt H 2 O 2 và HNO 3 đậm đặc Tro đen
Nung (nâng nhiệt từ từ đến 550 – 600 o C, 6 – 7h) Xử lý số liệu
Cân định lượng Cân định lượng Để nguội Cho 5g mẫu vào chén
Làm nguội, cân định lượng Để nguội, cân định lượng Nung (550 – 600 o C)
• Đặt chén vào tủ sấy ở 105 o C trong 3 h
• Làm nguội chén trong bình hút ẩm đến nhiệt độ phòng rồi cân chính xác khối lượng
• Tính phần trăm khối lượng của nước và tổng chất rắn trong sữa
3.3 Xác định độ tro của mẫu bột bắp
Sơ đồ 1.3 Quy trình xác định độ tro của mẫu bột bắp
• Nung chén sứ đã rửa sạch ở lò nung 550 – 600 o C đến trong lượng không đổi nhằm loại ẩm Để nguội ở bình hút ẩm và cân ở cân phân tích chính xác đến 0,001g
Cho khoảng 5g mẫu thử vào chén sứ và cân tất cả với độ chính xác cao Sau đó, đặt chén vào lò nung và nâng nhiệt độ từ từ cho đến 550 độ C.
• Nung cho đến tro trắng, nghĩa là đã loại hết các chất hữu cơ, thường khoảng 6 - 7 giờ
• Trường hợp còn tro đen, lấy ra để nguội, cho thêm vài giọt H2O2 hoặc – HNO3 đậm đặc và nung lại đến tro trắng
Để đảm bảo khối lượng ổn định và loại bỏ hoàn toàn độ ẩm xung quanh chén sứ, cần để nguội trong bình hút ẩm và cân đến độ chính xác Sau đó, tiếp tục nung ở nhiệt độ đã chỉ định trong 30 phút, rồi lại để nguội trong bình hút ẩm và cân cho đến khi trọng lượng không thay đổi.
Kết quả và xử lý số liệu
4.1 Xác định độ ẩm của mẫu bột bắp
Khối lượng đĩa và mẫu (trước khi sấy)
Khối lượng đĩa và mẫu (sau khi sấy)
Lần 1 Lần 2 Lần 3 Trung bình
Công thức tính độ ẩm:
% ẩm = 100 × (m H2O trong mẫu) / (m mẫu ướt)
% ẩm = 100 × [(m mẫu ướt + đĩa) – (m mẫu khô + đĩa)] / [(m mẫu ướt + đĩa) – (m đĩa)]
Hàm lượng ẩm trong mẫu 1: % ẩ𝑚 = 41.4197−41.1599 × 100% = 8.6500%
Hàm lượng ẩm trong mẫu 2: % ẩ𝑚 = 39.1877−38.9375 × 100% = 8.3294%
Hàm lượng ẩm trong mẫu 3: % ẩ𝑚 = 50.3508−50.1203 × 100% = 8.2428%
Hàm lượng ẩm trung bình trong mẫu bột bắp là:
4.2 Định lượng tổng chất rắn trong mẫu sữa lỏng (AOAC 990.19, 990.20)
Mẫu Khối lượng chén + nắp Khối lượng mẫu Khối lượng chén, nắp và mẫu (trước khi gia nhiệt)
Khối lượng chén, nắp và mẫu (sau khi sấy)
Lần 1 Lần 2 Lần 3 Trung bình
Công thức tính độ ẩm:
% ẩm = 100 × (m H2O trong mẫu) / (m mẫu ướt)
% ẩm = 100 × [(m mẫu ướt + đĩa) – (m mẫu khô + đĩa)] / [(m mẫu ướt + đĩa) – (m đĩa)]
Hàm lượng ẩm trong mẫu 1: % ẩ𝑚 = 69.1488−64.7365 × 100% = 88.1385%
Hàm lượng ẩm trong mẫu 2: % ẩ𝑚 = 70.6539−66.2372 × 100% = 88.2176%
Hàm lượng ẩm trung bình của sữa: % ẩm trung bình = 88.1385%+88.2176%
Công thức tính tổng chất rắn có trong sữa:
%mrắn= 100 × (mmẫu khô + đĩa − mđĩa)/(mmẫu ướt+chén+mchén) Hàm lượng tổng chất rắn của mẫu 1: %mrắn1= 64.7365−64.1427 × 100% = 11.8615%
Hàm lượng tổng chất rắn của mẫu 2: mrắn2= 66.2372−65.6473 × 100% = 11.7824%
Khối lượng tổng chất rắn trung bình của mẫu sữa: mrắn trung bình= 11.8615%+11.7824%
4.3 Xác định độ tro của mẫu bột bắp
Mẫu Khối lượng chén + nắp
Khối lượng chén, nắp và mẫu (trước khi nung)
Khối lượng chén, nắp và mẫu (sau khi nung)
Hàm lượng tro theo % được tính theo công thức:
X: % lượng tro trong mẫu sau khi nung G: trọng lượng chén (g)
G1: trong lượng chén và mẫu trước khi nung (g) G2: trong lượng chén và mẫu sau khi nung (g) Hàm lượng tro của mẫu 1: X1= 64.7285−64.7266 × 100% = 0.0380%
Hàm lượng tro của mẫu 2: X2 = 67.6634−67.6605 × 100% = 0.0580%
Hàm lượng tro trung bình của mẫu bột bắp: Xtb= 0.0380%+0.0580%
Bàn luận
Hình 1.4 Giá trị dinh dưỡng của bột bắp
5.1 Độ ẩm của mẫu bột bắp
Theo số liệu thực tế ghi trên nhãn, độ ẩm của bột bắp không vượt quá 14% Kết quả tính toán cho thấy độ ẩm đạt 8.4074%, thấp hơn mức tối đa cho phép, điều này cho thấy kết quả hoàn toàn phù hợp và chấp nhận được.
• Kết quả về hàm lượng ẩm trong mẫu bột bắp của các nhóm còn lại
Hàm lượng ẩm tính được
Trong ba nhóm, nhóm 2 có kết quả gần nhất với nhóm 4, với chênh lệch chỉ khoảng 0.0111% Nhóm 3 theo sau với sự chênh lệch 0.3642%, trong khi nhóm 1 có độ chênh lệch lớn nhất so với các nhóm còn lại, cụ thể là 1.6272% so với nhóm 4, 1.6383% so với nhóm 2, và 1.263% so với nhóm 3.
Kết quả của ba nhóm đều đạt mức chấp nhận được khi tỷ lệ không vượt quá 14% so với số liệu thực tế Sự khác biệt trong kết quả giữa các nhóm từ cùng một mẫu có thể được giải thích bởi nhiều yếu tố khách quan và chủ quan.
5.2 Định lượng tổng chất rắn trong mẫu sữa lỏng (AOAC 990.19, 990.20)
• Số liệu thực tế của mẫu sữa là 12%
Số liệu mà nhóm tính được là 11.8220%, với chênh lệch khoảng 0.1781% so với giá trị thực tế Sai số này không quá lớn và gần với giá trị thực tế, hoàn toàn có thể chấp nhận được.
• Kết quả về hàm lượng chất rắn có trong mẫu sữa của các nhóm còn lại
Hàm lượng ẩm trung bình của sữa được tính là 88.1781%, với sự chênh lệch không đáng kể giữa các nhóm Cả bốn nhóm đều cho thấy hàm lượng ẩm xấp xỉ 88%, trong đó độ chênh lệch lớn nhất là 0.2248% giữa nhóm 1 và nhóm 3, còn độ chênh lệch nhỏ nhất là 0.0873% giữa nhóm 4 và nhóm 2.
Tất cả bốn nhóm đều có hàm lượng rắn trong sữa khoảng 12%, gần với giá trị thực tế, cho thấy sự chênh lệch giữa các nhóm không lớn Điều này chứng tỏ sự chính xác và đồng đều trong thao tác của các nhóm.
5.3 Xác định độ tro trong mẫu bột bắp
• Số liệu thực tế ≤ 0.1% (dựa vào hình 1.4)
Hàm lượng tro trong mẫu bột bắp được xác định là 0.0480% (≤ 0.1%), đáp ứng tiêu chuẩn thực tế với độ chênh lệch khoảng 0.0520%, cho thấy con số này hoàn toàn chấp nhận được khi so sánh với dữ liệu thực tế.
• Kết quả của hàm lượng tro của các nhóm còn lại:
Hàm lượng tro tính được
Tất cả các nhóm đều đạt yêu cầu về hàm lượng tro từ thực nghiệm so với thực tế (≤ 0.1%), với sự chênh lệch cao nhất là 0.0249% giữa nhóm 4 và nhóm 3, và chênh lệch thấp nhất là 0.0081% giữa nhóm 2 và nhóm 3 Mặc dù sự chênh lệch này không lớn, nhưng so với hàm lượng tro thực tế, nó vẫn đáng kể Nguyên nhân của sự chênh lệch này có thể do những yếu tố khách quan hoặc chủ quan không mong muốn trong quá trình thực hiện thí nghiệm, chẳng hạn như môi trường và con người.
5.4 Nguyên nhân xảy ra sai số và biện pháp giảm sai số trong phòng thí nghiệm v Nguyên nhân:
• Sai số của thiết bị đo, cân, dụng cụ đo,…
• Sai số do thao tác của người thực hiện
• Do thời gian sấy, nung quá dài hoặc quá ngắn
• Quá trình sấy đĩa peptri, chén nung có thể chứ loại hoàn toàn ẩm
• Do điều kiện môi trường, ánh sáng, nhiệt độ phòng,…
• Hóa chất có thể lẫn tạp chất
• Có thể do pha sai nồng độ hóa chất,…… v Biện pháp:
• Sử dụng thành thạo các thiết bị cân, bình tam giác,… để giảm thiểu sai số do dụng cụ đo gây ra
• Lặp lại thí nghiệm ít nhất 3 lần trở lên
• Người thực hiện thí nghiệm yêu cầu phải cẩn thận, tỉ mỉ trong các thao tác thực hành
• Tính toán để pha dung dịch một cách chính xác (nên để nhiều người xem cách tính và kết quả, tránh phụ thuộc vào một người)
5.5 Mở rộng vấn đề Xác định độ ẩm bằng sấy đối lưu: v Ưu điểm:
• Chi phí thấp v Nhược điểm:
• Dễ làm bay hơi các chất mùi, màu, gây sai số
• Biến tính các thành phần trong quá trình sấy
Xác định độ tro bằng phương pháp tro hóa khô: v Ưu điểm:
• Có thể làm nhiều mẫu cùng một lúc v Nhược điểm:
• Thời gian tro hóa lâu
• Tổn thất các khoáng chất trong quá trình nung dẫn đến sai số lớn
• Hiện tượng tạp nhiễm dễ xảy ra do phương pháp lấy mẫu không phù hợp
Quy trình tiến hành thí nghiệm
Dụng cụ và thiết bị
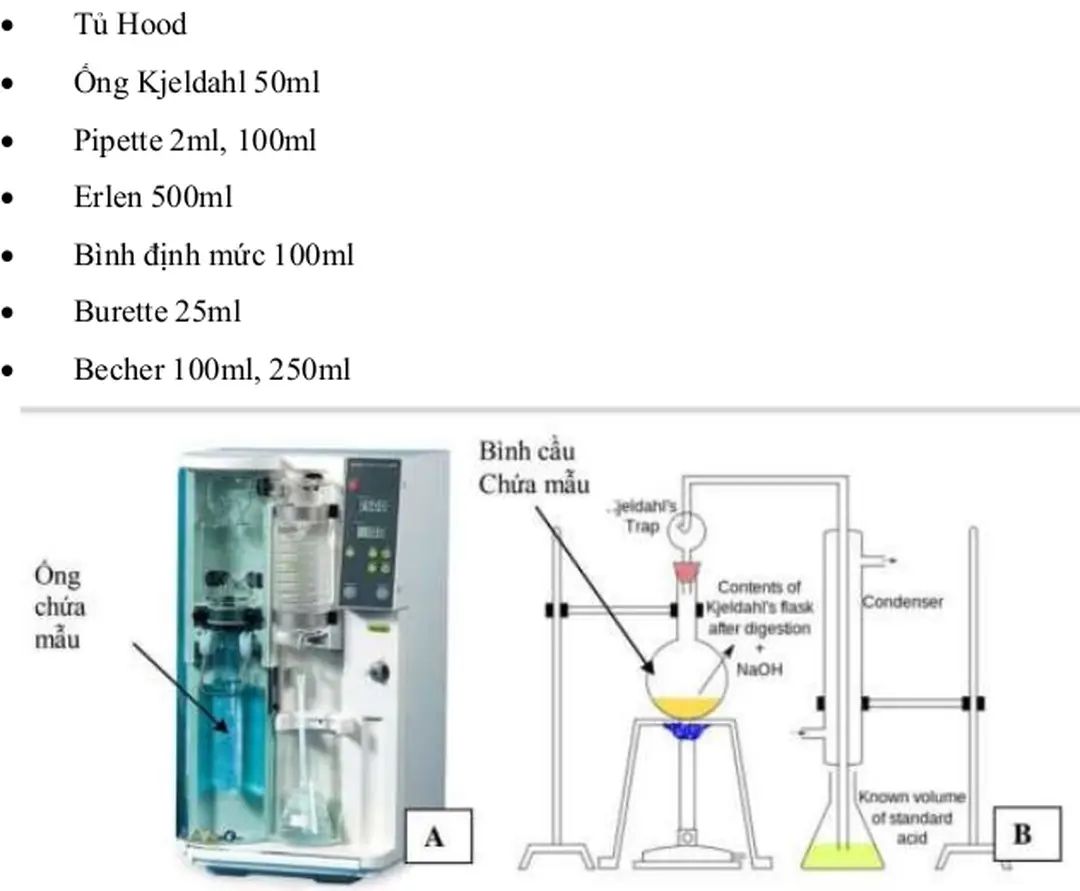
• Máy cất đạm bán tự động BUCHI
Hình 2.1.Máy BUCHI Distillation Unit (A) và nguyên tắc thiết bị tự lắp ráp (B) Mẫu thực phẩm và hóa chất
• H2SO4 đặc, NaOH 30%, HClO tinh khiết
Hình 2.2 Bịch sữa tươi không đường
5ml sữa, 5g K2SO4, 0.15g CuSO4, 0.15g TiO2, 20ml
Vô cơ hóa mẫu (1-2h) tùy mẫu
Chuyển mẫu vào bình định mức , thêm nước định mức lên 100ml
Lấy 10ml cho vào ống chứa mẫu, lắp vào hệ thống
Tính kết quả hàm lượng Nitơ tổng
Lấy erlen khỏi hệ thống, thêm 3 giọt phenolphtalein vào bình và định phân bằng
Sơ đồ 2.1 Định lượng Nito tổng bằng phương pháp Kjeldahl v Giải thích qui trình
Dùng pipet lấy 5mL sữa tươi, 5.0g K2SO4, 0.15g TiO4, 0.15g CuSO4 và cho thêm 15mL H2SO4 đậm đặc cho vào ống Kjeldahl
Sau đó đóng phần nắp phía trên ống Kjeldahl lại cho kín và tiến hành vô cơ hóa mẫu trong 3h
Trong quá trình vô cơ hóa mẫu, carbon và hydro sẽ được oxy hóa thành CO2 và H2O, trong khi nitơ được giải phóng dưới dạng NH3 kết hợp với H2SO4 tạo thành (NH4)2SO4 tan trong dung dịch Để tăng tốc độ của quá trình này, các chất xúc tác như K2SO4, CuSO4 và TiO2 được bổ sung.
Mục đích của quá trình này là oxi hóa các hợp chất hữu cơ, và để tăng tốc độ oxi hóa, cần bổ sung chất xúc tác K2SO4 giúp nâng cao nhiệt độ sôi, trong khi CuSO4 và TiO2 đóng vai trò quan trọng trong việc xúc tác cho phản ứng.
Trong quá trình vô chóa mẫu, nếu sử dụng bếp điện để đun trực tiếp bình Kjeldahl, cần thường xuyên lắc nhẹ và tráng khéo léo để đảm bảo không còn vết đen của mẫu nguyên liệu thí nghiệm chưa phân hủy bám lại trên thành bình Dừng lại khi dung dịch trong bình trở nên trong suốt và không còn vết than đen.
Sau khi vô cơ hóa mẫu trong 3 giờ, để nguội trong 30 phút Tiếp theo, chuyển toàn bộ mẫu vào bình định mức 100mL và thêm nước cho đến vạch 100mL Cuối cùng, lấy 10mL dung dịch thí nghiệm từ bình định mức và cho vào ống chứa mẫu hoặc bình.
Sau khi vô cơ hóa mẫu, cho NaOH vào hỗn hợp và đun nóng để tạo ra NH3 Khi hỗn hợp sôi, NH3 sẽ được cuốn theo và gặp sinh hàn, sau đó ngưng tụ và tác dụng với H2SO4.
Tiến hành cất đạm đến khi NH3 được giải phóng hoàn toàn khỏi bình chứa mẫu khoảng 15 phút
H2SO4 đậm đặc có tính háo nước cao và sinh nhiệt khi tiếp xúc với nước, điều này có thể dẫn đến sự bay hơi một phần và làm tăng thể tích dung dịch Do đó, cần phải làm nguội dung dịch để tránh sai số trong quá trình thao tác.
Cho 3 giọt phenolphtalein vào bình và định phân bằng NaOH 0.1N Định phân đến dung dịch trong bình chuyển thành màu hồng
4 4 Kết quả: v Số liệu dạng thô
Sữa,5ml Lần 1 Lần 2 Lần 3
17.8 18.1 17.9 v Tính toán kết quả và xử lí thống kê:
Công thức tính hàm lượng (%) Nito tổng
Hàm lượng Nito (N) được tính bằng phần trăm khối lượng, trong đó a là số mL dung dịch chuẩn H2SO4 0.1N dùng để hấp thụ NH3 (20ml), b là số mL dung dịch NaOH 0.1N sử dụng trong quá trình chuẩn độ, và m là thể tích/khối lượng mẫu đem vô cơ hóa (g/mL) (5ml) Tổng thể tích định mức dung dịch vô cơ hóa (V) là 100ml, trong khi v là thể tích dung dịch vô cơ hóa dùng để chưng cất (10ml) Mỗi 1mL H2SO4 0.1N tương ứng với 0.0014g Nito Hệ số hiệu chỉnh nồng độ NaOH 0.1N (K) được xác định là 1.
Hàm lượng Nito tổng trung bình trong mẫu sữa :
Hàm lượng protein trong sữa : P= %N x 6.38=0.579x6.38=3.694(g)
5 5 Bàn luận v Nhận xét kết quả và so sánh với số liệu thực tế:
Theo thí nghiệm, hàm lượng protein trong sữa đạt 3.694g, cao hơn so với mức công bố của nhà sản xuất là 3g/100ml, mặc dù có một số sai số Kết quả đo giữa các lần thực hiện cho thấy sự chênh lệch không đáng kể.
Hình 2.3 Giá trị dinh dưỡng của sữa tươi không đường Vinamilk v So sánh kết quả với các nhóm khác
Nhóm 1 có kết quả là 2.8582g/100ml Nhóm 2 có kết quả là 3.120g/100ml
Nhóm 3 có kết quả là 3.30g/100ml Nhóm 4 có kết quả là 3.694g/100ml
Có sự khác biệt giữa các nhóm thí nghiệm với giá trị trung bình khoảng 3±1 Trong đó, nhóm 1 có trọng lượng nhỏ hơn 3g, trong khi các nhóm 2, 3 và 4 đều lớn hơn 3g, với nhóm 4 ghi nhận sai số lớn nhất Tất cả các nhóm đều gặp phải sai sót, có thể do lỗi trong quá trình chuẩn bị thí nghiệm Các nguyên nhân gây ra sai số này đã ảnh hưởng đến kết quả cuối cùng của thí nghiệm.
• Sai số trong quá trình lấy mẫu (sai số do thiết bị)
• Tráng rửa dụng cụ không kỹ,còn lẫn tạp chất
• Định mức chưa đúng vạch ,không tráng kỹ dụng cụ đựng mẫu
Sai số khi định mức với acid H2SO4 đậm đặc háo nước có thể xảy ra do sự tỏa nhiệt mạnh, dẫn đến việc một phần nước bay hơi và làm cho thể tích dung dịch giãn nở.
• Lúc lắp ống nghiệm vào máy cất đạm không kỹ dẫn đến sự thất thoát mẫu
• Hóa chất chuẩn bị cho thí nghiệm không được chuẩn
• Thao tác đo không chính xác
• Hút hóa chất không chính xác v Cách khắc phục giảm thiểu sai số:
• Đong đo,tráng rửa dụng cụ cẩn thận
• Lấy hóa chất cẩn thận và chính xác hơn
• Thao tác dứt khoát và cẩn thận hơn
• Rèn kỹ năng nhạy: quan sát sự thay đổi màu tốt để dừng chuẩn độ đúng hơn, đọc kết quả chính xác hơn v Mở rộng vấn đề
Phương pháp Kjeldahl có nhiều ưu điểm như tính linh hoạt cho nhiều loại thực phẩm, chi phí hợp lý, và độ chính xác tương đối, đồng thời đã được cải tiến để xác định nồng độ protein thấp (microgram) Tuy nhiên, phương pháp này cũng tồn tại một số nhược điểm, bao gồm việc không thể cung cấp thước đo chính xác về protein thực sự do tất cả nitơ trong thực phẩm không chỉ tồn tại ở dạng nitơ, dẫn đến độ chính xác thấp.
Các phương pháp khác phân tích hàm lượng protein :
Phương pháp xác định hàm lượng protein trong mẫu dựa trên việc đốt cháy hoàn toàn mẫu bằng khí oxi tinh khiết ở nhiệt độ khoảng 950oC, tạo ra hỗn hợp khí gồm CO2, H2O, O2, NOx và N2 Sau quá trình đốt, hỗn hợp khí này được xử lý qua đồng kim loại và đồng oxit nóng đỏ, trong đó các oxit nitơ phân hủy thành nitơ và oxy Oxy này kết hợp với oxy trong khí đốt để tạo thành đồng oxit, trong khi cacbon oxit được oxy hóa thành cacbondioxit và hấp phụ vào dung dịch kiềm, để lại khí nitơ thoát ra Hàm lượng protein trong mẫu được tính toán dựa trên lượng khí nitơ đo được bằng nitơ kế Phương pháp này có nhiều ưu điểm như không sử dụng hóa chất độc hại, thực hiện nhanh chóng trong khoảng 3 phút, và có khả năng xác định tự động lên đến 150 mẫu mà không cần giám sát.
Nhược điểm: § Thiết bị mắc tiền § Chỉ đo được hàm lượng Nito tổng trong mẫu
Phương pháp Lowry là một kỹ thuật phân tích protein, kết hợp phản ứng biuret với phản ứng khử của dung dịch Folin-Ciocalteau, sử dụng phosphomolybdic và phosphotungstic acid Phương pháp này nhắm vào các gốc tyrosine và tryptophan trong phân tử protein, tạo ra phức màu xanh da trời, được đo ở bước sóng nhất định.
750 nm Cường độ màu của hỗn hợp phản ứng tỉ lệ thuận với nồng độ protein trong
Phương pháp xác định hàm lượng protein trong mẫu nghiên cứu dựa vào mức độ hấp thụ quang học của protein chuẩn cho thấy nhiều ưu điểm vượt trội Cụ thể, phương pháp này nhạy hơn thuốc thử Biuret từ 50 đến 100 lần và không bị ảnh hưởng bởi các tạp chất có trong sản phẩm.
Nhược điểm của các loại protein là chúng tạo ra màu sắc khác nhau, và mối quan hệ giữa nồng độ protein và cường độ màu không phải là tuyến tính Hơn nữa, các mẫu thực phẩm có nồng độ đường cao có thể phản ứng với thuốc thử, gây ảnh hưởng đến kết quả phân tích.
• Phương pháp Bicinchoninic Acid (BCA)
Mục đích thí nghiệm
• Hiểu rõ được quy trình định lượng protein hòa tan bằng phương pháp Biuret
• Sinh viên nắm vững các quy tắc cơ bản trong quá trình thí nghiệm
• Làm quen với thiết vị quang phổ UV – VIS
• Biết cách pha thuốc thử Biuret và bảo quản
Trong môi trường kiềm, mạch peptit kết hợp với Cu2+ tạo thành phức màu đặc trưng, với độ màu tăng theo hàm lượng protein Cường độ hấp thu của phức được đo ở bước sóng 540 nm, tỷ lệ thuận với nồng độ protein trong mẫu Hàm lượng protein hòa tan trong mẫu sẽ được xác định thông qua phương trình đường chuẩn.
Hình 3.1.Cấu trúc hợp chất phức giữa Cu 2+ và mạch peptit
Sơ đồ và trình tự tiến hành thí nghiệm
Mẫu dụng cụ và thiết bị
• Máy quang phổ UV – VIS
Mẫu thực phẩm và hóa chất
• Mẫu thực phẩm: Nước mắm
• NaOH v Cách pha thuốc thử Biuret
Để pha thuốc thử Biuret, đầu tiên hòa tan 0.375 g CuSO4.5H2O và 1.51 g natri kali tatrate (NaKC4H4O6) vào 100 mL nước, khuấy đều cho đến khi tan hoàn toàn Tiếp theo, bổ sung 100 mL dung dịch NaOH 10% vào hỗn hợp trên.
Thuốc thử Biuret Định mức lên
5 dung dịch protein chuẩn từ huyết thanh tương ứng
5 nồng độ 2, 4, 6, 8, 10 (mg protein/mL)
Cho vào từng ống nghiệm
Lắc đều (15 phút, t o phòng) Đo độ hấp thụ (bước sóng
Sau khi pha chế, hỗn hợp thuốc thử Biuret được định mức lên 250 mL và có thể sử dụng ngay lập tức Nếu không sử dụng ngay, thuốc thử cần được bảo quản trong lọ tối ở nhiệt độ từ 2 đến 8 độ C Thời gian bảo quản của thuốc thử Biuret thường kéo dài từ 15 đến 30 ngày.
• CuSO4.5H2O để cung cấp Cu 2+
• NaOH có vai trò tạo môi trường kiềm
• NaKC4H4O6 có vai trò giữ màu cho phức chất
Phương pháp này được sử dụng để xác định protein hòa tan trong các loại thực phẩm như ngũ cốc, đậu, thịt động vật và protein đậu nành tinh khiết.
3.1 Dựng đường chuẩn v Sơ đồ
Sơ đồ 3.2 Quy trình dựng đường chuẩn
Lấy 1 mL từng mȁu dung dịch
Xác định độ hấp thụ ở bước sóng 540 nm Xử lý số liệu v Giải thích quy trình:
Pha 5 dung dịch protein chuẩn từ huyết thanh bò (BSA) với nồng độ 2, 4, 6, 8 và 10 mg protein/mL Lấy 1 mL từng dung dịch protein chuẩn và thêm 5 mL thuốc thử biuret vào ống nghiệm Hỗn hợp được lắc đều trong 15 phút ở nhiệt độ phòng và sau đó đo độ hấp thu tại bước sóng 540 nm.
Đường chuẩn được vẽ với trục hoành biểu thị nồng độ protein và trục tung thể hiện độ hấp thụ Từ hàm lượng protein xác định trên đường chuẩn, ta có thể tính toán hàm lượng protein trong mẫu thử Việc sử dụng huyết thanh bò để dựng đường chuẩn thay vì dung dịch glucose là hợp lý, vì mục tiêu của thí nghiệm là xác định hàm lượng protein chứ không phải carbohydrate.
3.2 Xác định độ hấp thu của mẫu thực phẩm v Sơ đồ
Sơ đồ 3.3 Quy trình xác định độ hấp thụ của mẫu thực phẩm v Giải thích quy trình
Để trích ly protein từ mẫu rắn, cần lưu ý rằng nếu mẫu có chứa nhiều chất béo, phải tiến hành trích ly chất béo trước khi thực hiện trích ly protein.
36 nghiệm này, chúng ta sẽ tiến hành xác định hàm lượng protein trong mẫu nước mắm
• Sau đó, tiến hành pha loãng mẫu sao cho nồng độ protein trong mẫu nằm trong khoảng 2 – 10 mg/mL
Để tiến hành thí nghiệm, lấy 1 mL dịch trích và 5 mL thuốc thử biuret cho vào ống nghiệm, sau đó lắc đảo trong 15 phút ở nhiệt độ phòng Cuối cùng, xác định độ hấp thu của hỗn hợp ở bước sóng 540 nm.
• Giá trị nồng độ protein trong mẫu được xác định dựa vào phương trình đường chuẩn
Lưu ý: Huyết thanh bò rất đắt tiền, cần tính toán kĩ trước khi sử dụng
4 Kết quả và xử lý số liệu:
Bảng 3.1: Thành phần 7 ống nghiệm sử dụng trong thí nghiệm
Nồng độ BSA (mg/ml)
Bảng 3.2 Kết quả đo OD ở bước sóng 540nm
Hình 3.2 Đường chuẩn huyết thanh bò
Từ đường chuẩn trên hình ta có phương trình đường chuẩn dạng:
Ta có: Độ hấp thụ trung bình của mẫu:
Hàm lượng protein trung bình trong 1ml mẫu nước mắm là:
Hàm lượng protein hòa tan trong nước mắm thu được là 8,579 mg/ml
Số liệu thực tế: 10mg/ml
Như vậy kết quả thu được nhỏ hơn số liệu mà nhà sản xuất cung cấp do ảnh hưởng bởi các yếu tố dẫn đến sai số
• Nhóm 1: Hàm lượng protein hòa tan trong nước mắm thu được là 8,66mg/ml
• Nhóm 2: Hàm lượng protein hòa tan trong nước mắm thu được là 7,676 mg/mL
• Nhóm 3: Hàm lượng protein hòa tan trong nước mắm thu được là 8,244 mg/mL
Kết quả phân tích cho thấy nhóm 1, nhóm 3 và nhóm 4 có hàm lượng gần như tương đương nhau với các giá trị lần lượt là 8,66mg/ml, 8,244mg/ml và 8,579mg/ml, tất cả đều đạt trên 80% so với hàm lượng thực tế 10mg/ml Trong khi đó, nhóm 2 có hàm lượng thấp nhất là 7,676mg/ml nhưng vẫn đạt hơn 70% so với giá trị thực tế.
Do đó kết quả của 4 nhóm có sai số so với thực tế là do:
• Bước pha mẫu chưa thật sự chính xác
• Cân hóa chất chưa chính xác: do người cân, do môi trường
• Sai số trong các thiết bị và dụng cụ v Nguyên nhân gây sai số
• Mẫu protein chuẩn bị không được chuẩn
• Sai số trong quá trình thao tác lấy mẫu và pha loãng mẫu
• Ghi không chính xác chỉ số
Việc định mức hóa chất không chính xác và kỹ thuật đọc thể tích dung dịch không chuẩn có thể gây ra sự thiếu chính xác trong quá trình pha chế hóa chất cho thí nghiệm.
• Lắc chưa kĩ dung dịch
Curvet được sử dụng để đo độ hấp thụ của các chất không trong suốt và có bề mặt bị trầy xước, điều này có thể dẫn đến sai số trong quá trình đo Để giảm thiểu sai số này, cần áp dụng các phương pháp hiệu quả nhằm cải thiện độ chính xác của kết quả đo.
• Thao tác thí nghiệm cẩn thận và chính xác
• Đảm bảo các dụng cụ được vệ sinh sạch sẽ, không chứa tạp chất
• Hạn chế sai sót khi lấy và pha mẫu
• Lựa chọn những curvet trong suốt, không bị trầy xước, vệ sinh cuvette trước khi đo độ quang phổ v Mở rộng vấn đề:
• Ưu điểm của phương pháp Biuret: § Nhanh, đơn giản § Độ lệch màu ít § Xác định được hàm lượng protein hòa tan
Phương pháp Biuret có một số nhược điểm đáng lưu ý Đầu tiên, phương pháp này không hoàn toàn chính xác, vì lượng protein trong mẫu được xác định dựa trên đường chuẩn với huyết thanh bò Thứ hai, độ nhạy của phương pháp Biuret khá thấp, chỉ có thể phát hiện từ 2-4 mg protein Cuối cùng, màu sắc của phức chất có thể thay đổi tùy thuộc vào nguồn gốc của protein Ngoài phương pháp Biuret, còn có các phản ứng khác có thể được sử dụng để định tính và định lượng protein.
Phản ứng với thuốc thử Folin- Ciocalteau
Thuốc thử trong phương pháp Lowry sử dụng phản ứng biuret kết hợp với các bước và thuốc thử bổ sung để nâng cao độ nhạy phát hiện Phản ứng biuret cho phép đồng tương tác với bốn nguyên tử nitơ của peptide, tạo thành phức hợp đồng Phương pháp này sử dụng thuốc thử Folin-Ciocalteu, chứa axit phosphomolybdic/phosphotungstic, tương tác với các ion đồng và chuỗi bên của tyrosine, tryptophan và cysteine, tạo ra màu xanh lam có thể phát hiện trong khoảng 650nm-750nm Phạm vi phát hiện protein của phương pháp này là từ 5.
40 Ưu điểm của phương pháp Lowry: § Nhạy hơn phương pháp Biuret 50-100 lần § Không bị ảnh hưởng bởi các thành phần tạp chất trong thực phẩm
Nhược điểm § Các loại protein khác nhau cho màu sắc khác nhau § Nồng độ protein và cường độ màu không tuyến tính
Nhóm amin của axit amin tự do phản ứng với ninhydrin, một tác nhân oxy hóa, dẫn đến quá trình khử oxy hóa Quá trình này giải phóng CO2, NH3 và một aldehyde, cùng với hydrindantin, một dạng của ninhydrin Amoniac sau đó phản ứng với ninhydrin để tạo thành diketohydrin, hay còn gọi là phức hợp Ruhemann, có khả năng hấp thụ ánh sáng ở bước sóng 570nm.
Kết quả thí nghiệm cho thấy, amoniac cùng với các amin bậc 1 và bậc 2 tạo ra phức hợp có màu tím đậm Trong khi đó, hydroxyproline và proline tạo ra phức hợp màu vàng Đối với măng tây, phức hợp thu được có màu nâu.
Nếu không quan sát thấy sự thay đổi màu sắc, chất phân tích không chứa axit amin, amin hoặc amoniac.[2]
Thử nghiệm Xanthoproteic là phương pháp sử dụng phản ứng nitrate để xác định protein trong dung dịch Khi mẫu được xử lý bằng nitric acid đậm đặc và nóng, nó phản ứng với các amino acid thơm như phenylalanine, tyrosine và tryptophan, tạo ra sản phẩm màu vàng được gọi là protein Xantho Nếu bổ sung chất base mạnh như NH3 hoặc NaOH, màu sắc sẽ chuyển sang cam đậm hơn.
Mục đích bài thí nghiệm
Hơn 95% lipid trong thực phẩm là ester của các acid béo cao phân tử và glycerol, bao gồm dầu thực vật và mỡ động vật Ở động vật, lipid chủ yếu phân bố trong mô mỡ, não và sữa, trong khi ở thực vật, lipid thường tập trung ở hạt như đậu nành, đậu hộng, ô liu và hướng dương.
• Lipid không tan trong nước nhưng tan trong các dung môi hữu cơ không phân cực như toluen, benzen, cloroform,… v Mục đích
• Nhằm xác định lipid trong nguyên liệu hoặc sản phẩm thực phẩm dạng rắn bằng phương pháp trích ly với dung môi hữu cơ
• Sử dụng dung môi phù hợp với từng loại chất béo, ngoài ra giúp nắm đươc nguyên lý hoạt động của hệ thống Soxlet
Sử dụng dung môi kỵ nước để trích ly hoàn toàn lipid từ nguyên liệu đã được nghiền nhỏ, quá trình này cũng thu được một số thành phần hòa tan trong chất béo như hợp chất màu, vitamin tan trong chất béo và các chất mùi Tuy nhiên, hàm lượng của những thành phần này tương đối thấp, không gây ảnh hưởng đáng kể đến kết quả thu được Do sự hiện diện của tạp chất, sản phẩm trích ly được gọi là lipid tổng hay dầu thô.
Hàm lượng lipid tổng có thể được xác định bằng hai phương pháp: một là cân trực tiếp lượng dầu sau khi chưng cất và loại bỏ dung môi, hai là tính toán gián tiếp thông qua khối lượng bã còn lại sau quá trình này.
Trình tự tiến hành thí nghiệm
Dụng cụ và thiết bị
• Bộ Soxhlet (bình chứa dung môi, trụ chiết chứa mẫu, ống sinh hàn)
• Bộ Soxhlet (trụ chiết chứa mẫu và dung môi, ống sinh hàn)
• Cối chày sứ, bình hút ẩm
Mẫu thực phẩm và hóa chất
• Dung môi trích ly lipid: diethyl ether và petroleum ether v Sơ đồ
Mở nguồn nước làm lạnh ống sinh hàn Để ráo trong tủ Hood
Bật nguồn nhiệt làm bay hơi dung môi Lấy mẫu ra sau 8-12h
Sơ đồ 4.1 Định lượng Lipid tổng trong mẫu bằng phương pháp Soxlet Đổ dung môi vào trụ chiết
Sấy trong tủ sấy 102-104° trong 30 phút
1.0058g đậu phộng đã nghiền sấy
Cẩn xác định được khối lượng Để nguội trong bình hút ẩm Cho vào trụ chiết
Gói vào giấy chuyên dụng v Giải thích qui trình:
Nghiền nhỏ đậu phộng giúp tăng hiệu quả trích ly tăng diện tích tiếp xúc giữa mẫu và dung môi
Quá trình sấy mẫu trước khi bỏ vào trụ chiết diễn ra trong tủ sấy 105℃ trong vòng 30 phút sau đó để nguội khoảng 30 phút
Khi gói mẫu vào giấy chuyên dụng phải biết rõ khối lượng và đã được sấy khô
Trước khi lắp hệ thống Soxlet, lưu ý khởi động bể làm lạnh trước 15-20 phút.,
Cho túi giấy chứa mẫu vào trụ chiết và cho dung môi (petroleum ether và diethyl ether tỉ lệ 1:1) chảy qua trụ chiết xuống bình đựng dung môi Mở nguồn nước làm lạnh ống sinh hàn và đậy nắp bể điều nhiệt để tránh thất thoát nhiệt, gây quá tải bơm và hư hỏng hệ thống làm lạnh Bật nguồn nhiệt để dung môi bay hơi, sau đó dung môi bay hơi sẽ được làm lạnh, ngưng tụ và chảy xuống trụ chiết cũng như bình đựng dung môi Cần kiểm tra thường xuyên để đảm bảo không xảy ra lỗi hư hỏng không mong muốn.
Quá trình trích ly chất béo từ mẫu diễn ra trong khoảng 8 đến 12 giờ Sau khi trích ly, mẫu được sấy khô để loại bỏ hoàn toàn dung môi, đảm bảo cân chính xác lượng bã đậu còn lại.
Chúng ta có thể xác định điểm dừng của thí nghiệm bằng cách nhỏ vài giọt dung môi từ trụ chiết lên giấy lọc Nếu dung môi bay hơi mà không để lại vết dầu loang, điều này cho thấy thí nghiệm đã kết thúc.
Kết quả thí nghiệm
Mẫu Mẫu và giấy ban đầu M1
Mẫu và giấy sau khi trích ly lipid và sấy khô M2
Công thức tính khối lượng lipid :
M1 : Khối lượng túi giấy và mẫu ban đầu [g]
M2 : Khối lượng túi giấy và mẫu sau khi trích lipid và sấy khô [g] v Xử lý số liệu:
Hàm lượng lipid trích ly ra được có sự chênh lệch so với lí thuyết (49g lipid trong 100g đậu) v Kết quả của các nhóm khác
Kết quả trích ly chất béo từ bốn nhóm thí nghiệm đều cao hơn so với lượng chất béo lý thuyết trong hạt đậu phộng Nguyên nhân của sự chênh lệch này có thể do thao tác không chính xác trong quá trình thí nghiệm, sai số khi nghiền mẫu, hoặc do mẫu vẫn còn ẩm chưa được loại bỏ hoàn toàn.
• Có sự sai lệch này là do quá trình nghiền chưa đủ nhỏ
• Thời gian chỉ khoảng 6h, chưa đủ thời gian trích ly hoàn toàn mẫu
• Các sai số trong quá trình thực hiện như cân mẫu, trong quá trình thao tác v Biện pháp khắc phục
• Tăng thời gian trích ly
• Nghiền nhỏ mẫu để tăng diện tích tiếp xúc
• Trong quá trình thao tác thí nghiệm cần cẩn thận và chính xác
• Cần kiểm soát tốt ẩm trước khi trích ly béo v Mở rộng vấn đề
• Dựa vào tính tan hoàn toàn của chất béo vào dung môi hữu cơ
Sử dụng dung môi hữu cơ để trích ly chất béo từ sản phẩm thực phẩm, sau đó loại bỏ hoàn toàn dung môi bằng phương pháp bay hơi Cuối cùng, cân lượng chất béo còn lại để tính toán hàm lượng chất béo có trong sản phẩm thực phẩm.
• Chất béo phải tan hoàn toàn trong dung môi hữu cơ
• Có nhiệt độ sôi thấp hơn nhiều so với chất béo (có thể bay hơi ở nhiệt độ thường)
• Thường chọn các dung môi sau: diethyl ether , petroleum ether,… Ưu điểm:
• Có thể thu hồi được dung môi sau khi trích ly xong
• Thiết bị đơn giản, chi phí lắp đặt thấp
• Mất nhiều thời gian để xử lý mẫu trước khi trích ly
• Nhiều dung môi sử dụng có thể gây cháy nổ
Bộ môn Công nghệ Thực phẩm tại Khoa Công nghệ Hóa học và Thực phẩm, Trường ĐH Sư phạm Kỹ Thuật Tp.HCM cung cấp tài liệu hướng dẫn thí nghiệm phân tích thực phẩm, giúp sinh viên nắm vững kiến thức và kỹ năng cần thiết trong lĩnh vực này.
2 Reducing Sugars, Carbohydrate Classification and Properties R.F Tester, J Karkalas, in Encyclopedia of Food Sciences and Nutrition (Second Edition), 2003
Lê Thị Bích Dâ Nhóm 04
BÀI THÍ NGHIỆM SỐ 5: ĐỊNH LƯỢNG LIPID TỔNG TRONG MẪU LỎNG BẰNG PHƯƠNG PHÁP
Mục tiêu của bài thí nghiệm là xác định chất béo trong các loại thực phẩm dạng lỏng từ động vật như sữa bò, sữa dê, sữa cừu và từ thực vật như sữa dừa và sữa dầu cọ Các chất béo này phân bố dưới dạng hạt cầu, được bao bọc và nhũ hóa bởi lớp màng phospholipid và protein Để đạt độ chính xác cao trong việc xác định chất béo, cần loại bỏ lớp protein bảo vệ trước khi trích ly chất béo bằng dung môi hữu cơ.
Hiểu biết về lý thuyết trích ly chất béo trong sản phẩm thực phẩm dạng lỏng, đặc biệt là sữa động vật và thực vật, là rất quan trọng Ứng dụng lý thuyết này giúp xác định tổng lượng béo trong dịch sữa dừa thông qua phương pháp Adam Rose – Gottlieb cải tiến.
• Rèn luyện kỹ thuật thực hành, sử dụng các loại dụng cụ, rèn luyện kỹ năng làm việc trong phòng thí nghiệm
• Biết cách sử dụng của các dụng cụ để xác định lượng lipid
Để thực hiện thí nghiệm hiệu quả, cần nắm rõ nguyên tắc và trình tự tiến hành, cũng như tính toán và đánh giá kết quả Bên cạnh đó, việc xác định sai số và các yếu tố ảnh hưởng đến kết quả thí nghiệm cũng rất quan trọng.
Chất béo trong mẫu sữa được trích ly qua việc sử dụng bốn dung môi khác nhau: amoniac, cồn, diethy ether và petroleum ether Trong quá trình này, cồn và amoniac giúp loại bỏ protein khỏi các hạt cầu béo, trong khi diethy ether và petroleum ether được sử dụng để trích ly chất béo và các thành phần hòa tan trong chất béo.
Sau khi bổ sung dung môi và khuấy đều, hỗn hợp tách thành hai pha: pha nhẹ ở trên chứa dung môi và chất béo, trong khi pha nặng dưới gồm nước và các chất hòa tan Pha nhẹ này được thu lại, sau đó dung môi được bay hơi để thu được tổng lượng chất béo trong mẫu sữa.
Quy trình thực hiện
Vật liệu, dụng cụ và thiết bị:
• Dịch sữa (trong bài thí nghiệm này sử dụng nguyên liệu là nước cốt dừa hay còn gọi là sữa dừa): Sản phẩm Nước cốt dừa WONDERFARM
• Dung dịch NH3 đậm đặc (25%)
Dụng cụ và thiết bị:
• Đĩa petri Hình 5.1 Phễu chiết thủy tinh
25ml petroleum Chuyển hỗn hợp vào phễu chiết
25ml diethyethe Lắc đều trong 5 phút
Pha nặng Thu pha nhẹ vào đĩa petri
Chiết Để yên trong 30 phút Đun nhẹ
• Cân định lượng (4 số lẻ)
• Bình hút ẩm v Sơ đồ:
Sơ đồ 5.1 Quy trình định lượng lipid tổng trong mẫu lỏng bằng phương pháp Adam Rose-Gottlieb
10ml cồn Lắc đều trong 1 phút
Lấy 10ml dịch sữa cho vào erlen 250ml
Tráng erlen bằng petroleum erther
Để loại bỏ protein khỏi các hạt cầu béo trong sữa dừa, cần bổ sung lần lượt 1.5 mL dung dịch NH3 và 10 mL cồn NH3 có tác dụng phá vỡ cấu trúc hạt cầu béo và lớp protein, trong khi cồn giúp kết tủa protein.
Lắc đều hỗn hợp trong 1 phút, sau đó thêm 25 mL diethyl ether và lắc trong 5 phút Cuối cùng, bổ sung 25 mL petroleum ether và lắc đều trong 5 phút để trích ly chất béo và các thành phần tan trong chất béo Diethyl ether là dung môi trích ly hiệu quả cho cả phần phân cực và không phân cực, trong khi petroleum ether chỉ trích ly chất béo không phân cực Mặc dù petroleum ether có tính chọn lọc cao hơn, nhưng hiệu suất trích ly của nó thấp hơn diethyl ether, vì vậy việc kết hợp cả hai dung môi là cần thiết.
2 dung môi với nhau để tăng hiệu quả trích ly
Chuyển toàn bộ hỗn hợp mẫu và dung môi vào phễu chiết, sau đó tráng erlen bằng petroleum ether nhiều lần để đảm bảo trích ly hết lượng béo còn sót lại trên thành erlen.
Cho toàn bộ hỗn hợp vào phễu chiết và để quá trình tách lớp tự nhiên trong 30 phút Hỗn hợp sẽ phân tách thành hai pha: pha nhẹ chứa dung môi diethyl ether, petroleum ether và béo, trong khi pha nặng bao gồm protein kết tủa, cồn, NH3 và các thành phần còn lại trong sữa.
Để loại bỏ dung môi diethyl ether và petroleum ether, hãy thu pha nhẹ và đặt vào đĩa petri Tiến hành đun nóng nhẹ đĩa petri trong tủ hút hoặc để cho khô tự nhiên.
Đặt đĩa petri vào tủ sấy ở nhiệt độ 102±1oC và sấy cho đến khi đạt khối lượng không đổi, khoảng 1 giờ Quá trình này giúp loại bỏ hoàn toàn các dung môi và nước còn sót lại trong đĩa petri.
Sau khi đĩa petri chứa béo đã được làm nguội trong bình hút ẩm đến nhiệt độ phòng, cần tiến hành cân định lượng Việc này giúp tránh hiện tượng hút ẩm trở lại vào đĩa, đảm bảo độ chính xác của kết quả.
Kết quả
Khối lượng đĩa petri (m) 37,0326g Khối lượng đĩa và mẫu sau sấy (M) 38,3108g v Tính toán kết quả và xử lý thống kê:
Hàm lượng chất béo có trong 100 mL dịch sữa được tính theo công thức sau:
Hàm lượng tổng chất béo (TF) trong 100 mL dịch sữa được tính bằng gam trên 100 mL Để xác định TF, cần đo khối lượng đĩa petri và chất béo sau khi sấy, sau đó trừ đi khối lượng đĩa petri ban đầu Thể tích sữa được phân tích là 10 mL.
Hàm lượng chất béo trong dịch sữa dừa theo kết quả thí nghiệm là 12,782g/100ml
Dựa vào kết quả nghiên cứu, chúng tôi xác định được lượng chất béo có trong
Trong 100 mL sữa dừa, hàm lượng chất béo được xác định là 12,782 g, trong khi giá trị ghi trên nhãn là 14,1 g/100 mL Kết quả này cho thấy hàm lượng thực tế thấp hơn 8,46 g/100 mL, tương đương giảm hơn 60%.
• Nhóm 1: 14,104g/100mL (so với 14,1g/100mL)
• Nhóm 2: 12,6110g/100mL (so với 14,1g/100mL)
• Nhóm 3: 12,296g/100mL (so với 14,1g/100mL)
So với giá trị chất béo thực tế trên lon sản phẩm, cả 4 nhóm đều đạt tỷ lệ trên 60% Đặc biệt, nhóm 1 có kết quả vượt mức giá trị thực tế với 0,004g/100ml chất béo Nguyên nhân của sai số này cần được xem xét kỹ lưỡng.
• Thao tác chưa chính xác, sai sót trong quá trình lấy mẫu, lắc không đều dẫn đến sai số so với kết quả thực tế.
• Quá trình trích ly chưa hoàn toàn, sót lại một phần ở phễu chiết hay erlen do pha nhẹ không nổi lên trong quá trình trích ly
• Các sai số trong quá trình cân đĩa, câu mẫu.
• Do mẫu sản phẩm được trữ lạnh quá lâu (2 tháng) có thể ảnh hưởng tới cấu trúc, chất béo của sản phẩm. v Cách khắc phục
Các loai dung môi đều có yêu cầu chung:
• Hòa tan chất béo tốt
• Không ăn mòn thiết bị, không gây độc hại, dễ tìm và giá thành rẻ [2]
Muốn rút ngắn thời gian trích ly ta cần:
• Chọn nhiệt độ phù hợp, nhiệt độ cao thì các phân tử béo khuếch tán nhanh vào dung môi
• Trước khi trích ly, ta cần loại bỏ lớp protein bảo vệ ở các hạt cầu béo v Mở rộng
Dung dịch H2SO4 đậm đặc sẽ kết tủa protein, giải phóng các hạt cầu béo có xu hướng kết dính lại và tạo thành khối lớn Sau đó, tiến hành ly tâm và bổ sung nước nóng để các cầu béo nổi lên cổ chai Babcook Cuối cùng, xác định thể tích chất béo bằng vạch đo trên cổ chai.
• Ưu điểm: Đơn giản dễ thực hiện, nhanh
• Nhược điểm: § H2SO4 đậm đặc dễ gây cháy, nguy hiểm § Không xác định được phospholipid § Không phù hợp với các mẫu sản phẩm chứa nhiều đường, chocolate,
• Nguyên tắc: Tương tự như phương pháp Babcock, sử dụng 2 loại hóa chất H2SO4 đậm đặc và iso amyl alcohol
Phương pháp này có nhiều ưu điểm như tính đơn giản và dễ thực hiện, nhanh hơn so với phương pháp Babcock Ngoài ra, việc đọc vạch chất béo trở nên dễ dàng hơn nhờ vào việc sử dụng isoamyl alcohol, đồng thời ngăn chặn phản ứng đốt cháy đối với các sản phẩm chứa đường, chocolate và các thành phần khác.
• Nhược điểm: Sử dụng acid dễ cháy nổ, nguy hiểm.[2]
Bộ môn công nghệ thực phẩm tại Khoa Công nghệ Hóa học và Thực phẩm, Trường ĐH Sư phạm Kỹ Thuật Tp.HCM cung cấp tài liệu hướng dẫn thí nghiệm phân tích thực phẩm.
2 Reducing Sugars, Carbohydrate Classification and Properties R.F Tester, J Karkalas, in Encyclopedia of Food Sciences and Nutrition (Second Edition), 2003
Lê Thị Bích Dâ Nhóm 04
BÁO CÁO THÍ NGHIỆM SỐ 6: ĐỊNH LƯỢNG ĐƯỜNG KHỬ BẰNG PHƯƠNG PHÁP QUANG PHỔ SO
MÀU VỚI THUỐC THỬ DNS
Mục tiêu của bài thí nghiệm là tìm hiểu về đường khử, bao gồm các loại đường có nhóm aldehyde (-CHO) hoặc ketone (-CO) như glucose, fructose, arabinose, maltose và lactose Đặc biệt, sucrose (đường mía) và trehalose không được coi là đường khử.
Có nhiều phương pháp xác định hàm lượng đường khử, bao gồm phương pháp Somogyi-Nelson, phương pháp quang phổ so màu với thuốc thử Acis Dinitro-Salicylic (DNS), phương pháp chuẩn độ oxy hóa khử với Kali Ferrycyanure và phương pháp The Munsin-Walker (AOAC method 906.03) Trong số đó, phương pháp quang phổ so màu bằng thuốc thử DNS nổi bật nhờ sử dụng hóa chất đơn giản, dễ thực hiện và thao tác đơn giản, đồng thời mang lại kết quả chính xác cao.
Phương pháp quang phổ dựa trên sự biến đổi của bức xạ điện từ khi tương tác với vật chất, trong đó cường độ tia sáng đơn sắc giảm khi đi qua dung dịch màu Mức độ giảm cường độ này, tương ứng với nồng độ chất tan, tuân theo định luật Beer – Lambert, cho phép xác định nồng độ chất tan trong dung dịch Để định luật này được áp dụng chính xác, cần đảm bảo bức xạ là đơn sắc, nồng độ dung dịch [C] nhỏ hơn 0,01M và độ hấp thu A nằm trong khoảng 0,2-0,8 hoặc A nhỏ hơn 3,0 Mục tiêu của bài thí nghiệm là kiểm tra các yếu tố này.
• Làm quen với cấu tạo, nguyên lý hoạt động của thiết bị quang phổ so màu UV-VIS
• Sử dụng thiết bị quang phổ để xác định nồng độ đường khử bằng phương pháp so màu sau khi cho phản ứng với thuốc thử DNS (3,5-Dinitrosalicylic acid)
Phương pháp này sử dụng phản ứng tạo màu giữa đường khử và thuốc thử DNS để xác định cường độ màu của hợp chất bằng thiết bị quang phổ UV-Vis Cường độ màu tỉ lệ thuận với nồng độ đường khử trong một phạm vi nhất định, cho phép xác định hàm lượng đường khử của mẫu thí nghiệm thông qua phương trình đường chuẩn.
3 Sơ đồ trình tự tiến hành thí nghiệm:
Dụng cụ, thiết bị , mẫu thực phẩm và hóa chất :
• Pipette 1mL ,2mL và 5mL
Thiết bị : Máy quang phổ so màu UV-VIS
Hình 6.1 Thiết bị quang phổ so màu UV-VIS ( ảnh minh họa )
Mẫu thực phẩm : Mẫu nước cam có tép Teppy
Hình 6.2 Nước cam được sử dụng làm mẫu Hóa chất :
• Thuốc thử DNS bao gồm : § Nước cất: 60 – 70mL § NaOH rắn: 1,6g § DNS (C7H4N2O7): 1g § Muối natrikali tartrat (KNaC4H4O4.4H2O): 30g
Hỗn hợp cần được khuấy đều bằng máy khuấy từ và định mức đến vạch 100mL trong bình định mức Thuốc thử nên được bảo quản ở nhiệt độ thấp từ 2 – 8oC và trong điều kiện không có ánh sáng, với dung dịch vẫn đảm bảo chất lượng sử dụng trong khoảng 10 – 14 ngày.
STT ống nghiệm ĐC 1 2 3 4 5 Mẫu 1 Mẫu 2
Bảng 6.1 Thành phần dãy ống nghiệm trong phương pháp quang phổ so màu với thuốc thử DNS
Sơ đồ 6.1 Sơ đồ quy trình định lượng đường khử bằng phương pháp so màu với thuốc thử DNS
O,1g Glucose Định mức 100ml , lắc đều
Pha loãng 100 lần Lọc bỏ tép
Pha theo tỉ lệ bảng 5.1 vào các ống nghiệm
Thiết lập đường chuẩn, tính toán Đun sôi cách thủy trong 5 phút
Cho 2-3ml mȁu vào Cuvette Làm nguội nhanh đến nhiệt độ phòng Đo mật độ quang ở bước sóng 540nm
1,6g NaOH rắn Định mức 100ml và khuấy tan
Để chuẩn bị dung dịch mẫu, nước cam sau khi đã lọc bỏ tép được pha loãng với tỷ lệ 1:100 Cụ thể, sử dụng micropipette để hút 1ml nước cam và cho vào bình định mức, sau đó thêm nước để định mức lên 100ml, từ đó thu được dung dịch mẫu.
• Pha dung dịch glucose chuẩn 0.1% : Cân 0.1g Glucose định mức đến 100ml , lắc đều thu được dung dịch glucose chuẩn 0.1%
Để pha thuốc thử DNS, cần sử dụng hỗn hợp gồm 30g KNaC4H4O4.4H2O, 1g DNS (C7H4N2O7) và 1,6g NaOH rắn hòa tan trong 60-70ml nước cất Khuấy đều hỗn hợp bằng máy khuấy từ cho đến khi tan hoàn toàn, sau đó định mức đến vạch 100ml Thuốc thử này nên được bảo quản ở nhiệt độ thấp từ 2-8 độ C và tránh ánh sáng.
• Pha theo tỉ lệ bảng 5.1 : Chuẩn bị các ống nghiệm rồi rót các dung dịch theo tỉ lệ như bảng 5.1
• Đun cách thủy : Để phản ứng giữa đường khử và thuốc thử DNS xảy ra
• Làm nguội : Hạ nhiệt độ xuống nhiệt độ phòng
• Dùng micropipette hút từ 2-3ml mẫu trong ống nghiệm cho vào Cuvette rồi tiến hành đo mật độ quang ở bước song 540nm bằng thiết bị quang phổ so màu
Dựa trên số liệu thu thập được, chúng tôi đã xây dựng đồ thị thể hiện mối quan hệ giữa nồng độ đường khử và độ hấp thu được xác định bằng thiết bị quang phổ so màu.
• Viết phương trình đường chuẩn : A= f(C ), xác định hệ số tương quan R
4 Kết quả : v Số liệu dạng thô :
Bảng 6.2 Kết quả thu được sau khi đo mẫu bằng máy quang phổ UV-VIS 540nm
Hình 6.3 Dãy ống nghiệm chứa mẫu đối chứng và các mẫu từ 1đến 7 ( trong đó số 6,7 là 2 mẫu chứa dung dịch mẫu ) theo thứ tự từ trái sang phải
Hình 6.4 minh họa quá trình chuyển các mẫu vào Cuvette theo thứ tự từ mẫu ĐC đến mẫu 2, đồng thời đồ thị thể hiện mối quan hệ giữa nồng độ đường khử và độ hấp thụ OD.
Hàm lượng đường khử mg/ml y = 0.3 486x - 0.0102
Hình 6.5 Đồ thị thể hiện mối quan hệ giữa nồng độ đường khử và độ hấp thụ OD 540nm
(đường chuẩn của nồng độ đường khử) v Tính toán kết quả và xử lí thống kê:
Theo phương trình tuyến tính giữa nồng độ đường khử và mật độ quang thì ta có : y = 0.3486x-0.0102
Mẫu 1 : ta có ytb=0.395 => x= 0.395+0.0102 =1.162 (mg/ml)
Hàm lượng đường trong mẫu 1 là = 1.162×100×100 = 11.62(g)
Mẫu 2 : ta có ytb = 0.393 => x=0.393+0.0102= 1.157( mg/ml)
Hàm lượng đường trong mẫu 2 là =1.157×100×100 57(g)
1000 ð Hàm lượng đường khử trung bình là :