PHA TẠP ĐẤT HIẾM
VẬT LIỆU TIO 2
1.1.1 Cấu trúc vật liệu TiO 2
Titanium dioxide (TiO2), hay còn gọi là titan (IV) oxit, là một loại bán dẫn hình thành ở nhiệt độ cao khi Ti phản ứng với O, có trọng lượng phân tử 79,87 g/mol TiO2 có trạng thái oxi hóa bền nhất là +4, với cấu hình điện tử giống khí hiếm, trong khi Ti cũng có thể tồn tại ở các trạng thái +2 và +3 nhưng dễ chuyển sang trạng thái +4 bền hơn TiO2 ở kích thước micro rất bền về mặt hóa học, trong khi dạng nano có khả năng phản ứng với axit mạnh Các dạng oxit, hydroxit và hợp chất của Ti (IV) đều có tính chất lưỡng tính, và TiO2 sở hữu nhiều tính năng ưu việt, thích hợp cho ứng dụng làm chất quang xúc tác.
TiO2 có ba dạng đa hình chính: brookite, rutile và anatase Trong tự nhiên, brookite phong phú nhưng không ổn định, dễ chuyển đổi sang các pha khác Anatase và rutile là hai dạng phổ biến và được nghiên cứu nhiều nhất, trong đó rutile là pha ổn định nhất, hình thành ở nhiệt độ cao, còn anatase được hình thành ở nhiệt độ thấp hơn, khoảng 450°C.
Giai đoạn chuyển đổi không thể đảo ngược từ anatase sang pha rutile xảy ra ở nhiệt độ cao, liên quan đến sự vỡ và hình thành các liên kết mới Quá trình chuyển đổi này không chỉ phụ thuộc vào nhiệt độ mà còn bị ảnh hưởng bởi phương pháp tổng hợp, hình dạng và kích thước hạt của anatase.
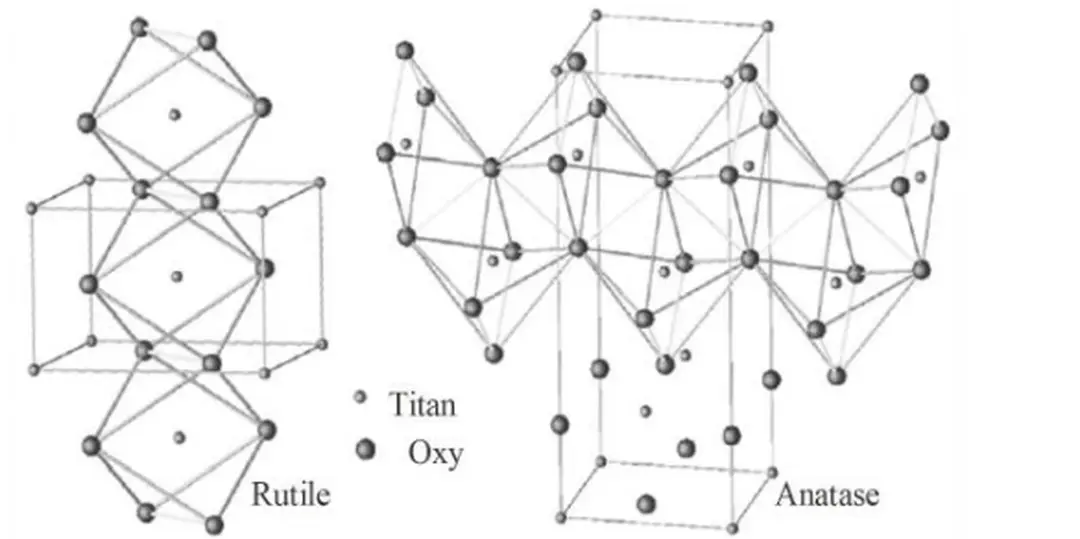
Hình 1.1 Tế bào đơn vị của rutile, anatase và brookite (từ trái sang phải)
Bảng 1.1 Tính chất tinh thể học của rutil, anatase và brookite
Các đơn vị cấu trúc cơ bản trong ba tinh thể TiO2 bao gồm bát diện TiO6, với các chế độ sắp xếp khác nhau Trong dạng rutil, bát diện TiO6 liên kết bằng cách chia sẻ một cạnh dọc theo trục c, tạo thành các chuỗi liên kết với nhau qua các nguyên tử oxy ở góc, hình thành một khung ba chiều Ngược lại, trong anatase, khung ba chiều được tạo ra từ liên kết chia sẻ cạnh giữa các bát diện TiO6, dẫn đến cấu trúc chuỗi ngoằn ngoèo với bốn cạnh Trong khi đó, brookite có cấu trúc hình thoi với các bát diện chia sẻ cả cạnh và góc.
Cấu trúc của hai pha TiO2, anatase và rutile, được phân loại theo nhóm không gian I41/amd và P42/mnm, tương ứng Sự khác biệt giữa hai cấu trúc này nằm ở biến dạng của khối bát diện TiO6 và cách thức liên kết giữa chúng Trong pha anatase, mỗi ion Ti4+ được bao quanh bởi 6 ion O2-, tạo thành cấu trúc bát diện đặc trưng.
5 khoảng cách 1,94 Å từ titan và hai oxy còn lại ở 1,99 Å Trong pha rutile có bốn oxy ở khoảng cách 1,95 Å và hai oxy tại 1,98 Å [9]
Thông số điện tử và tính chất như độ hòa tan, độ cứng của TiO2 anatase và rutile, hiển thị trong bảng 1.2
Bảng 1.2 Các thông số đặc trưng của TiO2 anatase và rutile [9]
Thông số Pha Anatase Pha Rutile
Cấu trúc tinh thể Tetragonal Tetragonal
Số nguyên tử trên tế bào đơn nhất Z
Nhóm không gian I41/amd P42/mnm
Thông số mạng (Å) a = 3,785 c = 9,515 a = 4,594 c = 2,959 Thể tích đơn vị tế bào (Å 3 ) 136,300 62,499
Eg tính toán trực tiếp
Hòa tan trong axit HF Hòa tan Không hòa tan
Hòa tan trong nước Không hòa tan Không hòa tan Độ cứng (Mohs) 5,5 - 6 6 – 6,5
Kỹ thuật nhiễu xạ tia X (XRD) được sử dụng để xác định cấu trúc tinh thể và kích thước hạt của ba dạng tinh thể chính: anatase, rutil và brookite Các đỉnh nhiễu xạ của anatase xuất hiện ở các góc θ = 12,65°, 18,9° và 24,054°, trong khi đỉnh của rutil được tìm thấy ở θ = 13,75°, 18,1° và 27,2° Đỉnh của brookite xuất hiện tại các góc θ = 12,65°, 12,85°, 15,4° và 18,1°.
Kỹ thuật phổ tán xạ Raman là phương pháp hiệu quả để xác định cấu trúc tinh thể của TiO2 thông qua các đỉnh đặc trưng Anatase có tổng cộng sáu chế độ hoạt động Raman, bao gồm A1g, hai chế độ B1g và ba chế độ Eg Ba chế độ Eg nằm trong khoảng từ 144 cm^-1 đến 197 cm^-1.
1 và 640 cm -1 [được chỉ định ở đây Eg(1), Eg (2) và Eg (3)]; hai chế độ B1g ở mức
Chế độ Raman mạnh nhất của anatase TiO2 là Eg(1), tương ứng với mạng đối xứng rung động góc Trong khi đó, rutile có bốn chế độ hoạt động Raman: A1g, B2g, Eg, và B1g, được phát hiện tại các vị trí xung quanh 400 và 515 cm-1, được chỉ định là B1g(1) và B1g(2) Do vị trí của A1g và B1g(2) gần giống nhau, nên không cần phân biệt rõ ràng giữa chúng.
B1g: 143 cm -1 ; Eg: 447 cm -1 ; A1g: 612 cm -1 ; và B2g: 826 cm -1 Với cường độ mạnh hơn nhiều, Eg và A1g được gọi là các đỉnh đặc trưng của TiO2 rutile [8].
1.1.2 Cấu trúc vùng năng lượng của TiO 2
TiO2 là một bán dẫn với độ rộng vùng cấm lớn, trong đó vùng hóa trị được lấp đầy electron và vùng dẫn hoàn toàn trống TiO2 ở pha anatase có độ rộng vùng cấm khoảng 3,2 eV, tương ứng với bước sóng ánh sáng khoảng 388 nm, trong khi TiO2 pha rutile có độ rộng vùng cấm khoảng 3,0 eV, tương ứng với bước sóng khoảng 413 nm.
Hình 1.3 Giản đồ vùng năng lượng của TiO2
1.1.3 Một số ứng dụng của vật liệu TiO 2 nano
Gần đây, vật liệu nano TiO2 có kích thước nhỏ hơn 100 nm đã được chế tạo thành công với nhiều dạng thù hình như hình cầu, ống nano, thanh nano, dây nano, tấm nano và sợi nano Bảng 1.3 tổng hợp các ứng dụng tiềm năng của vật liệu nano TiO2.
Bảng 1.3 Các ứng dụng phổ biến của vật liệu TiO2 cấu trúc nano Ứng dụng Ví dụ
Tế bào quang điện Dye – sensitized solars cell
Sản xuất và lưu trữ khí hidro Sản xuất hidro từ nước biển
Cảm biến Cảm biến độ ẩm, H2O2, VOC, CH3, oxy và hidro
Pin Pin lithium có khả năng điều trị và ngăn ngừa ung thư nhờ vào tác dụng ức chế tế bào ung thư Ngoài ra, sản phẩm này còn có tính năng kháng khuẩn và tự làm sạch, rất phù hợp cho việc sử dụng trong các tòa nhà cao tầng và phòng bệnh.
Các thiết bị điện Đèn led
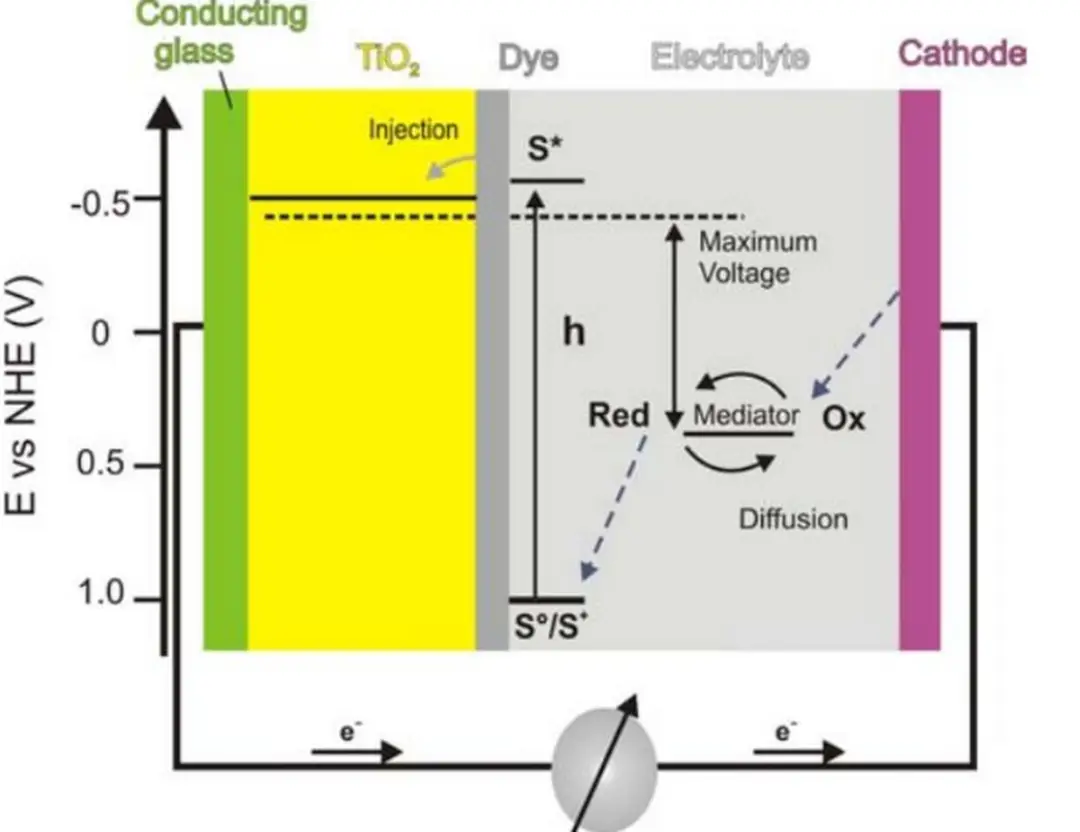
Pin mặt trời nhạy cảm với thuốc nhuộm (DSSC) bao gồm hai lớp kính dẫn điện, màng TiO2 nhạy cảm với thuốc nhuộm ruthenium, lớp xúc tác bạch kim và chất điện phân lỏng chứa cặp đôi iodua/triiodide Hệ thống này hoạt động bằng cách quang kích thích thuốc nhuộm, tạo ra điện tử trong vùng dẫn của TiO2, cho phép điện tử di chuyển ra mạch ngoài để tạo ra năng lượng điện Sau khi điện tử được truyền ra, trạng thái ban đầu của thuốc nhuộm được phục hồi thông qua sự khử từ chất điện phân Quá trình này giúp ngăn chặn sự thu hồi điện tử từ thuốc nhuộm đã bị oxy hóa, với iodide được tái tạo tại điện cực đối, hoàn tất mạch điện qua sự di chuyển điện tử Điện áp được tạo ra dưới ánh sáng phụ thuộc vào sự khác biệt giữa mức Fermi của TiO2 và thế oxy hóa khử của chất điện phân.
Khi pin mặt trời TiO2 tiếp xúc với ánh sáng, ba phản ứng chính xảy ra, bao gồm sự chuyển điện tử từ trạng thái kích thích của thuốc nhuộm sang vùng dẫn của TiO2.
(b) quá trình đưa điện tử nóng hoặc quá trình thư giản / làm mát của điện tử nóng trong vùng dẫn và ở trạng thái bẫy,
(c) sự tái tổ hợp giữa điện tử vùng dẫn và cation thuốc nhuộm và / hoặc bắt giữ bởi các bẫy [5,17,18]
Hình 1.5 Nguyên lý hoạt động của DSSC
Cơ chế sản xuất hydro thông qua quá trình quang xúc tác bởi TiO2 được minh họa trong hình 1.6 Khi chất bán dẫn TiO2 hấp thụ photon có năng lượng bằng hoặc lớn hơn mức năng lượng vùng cấm, các electron sẽ nhận năng lượng và được kích thích từ vùng hóa trị (VB) lên vùng dẫn (CB) Phản ứng này của TiO2 được mô tả bằng các phương trình cụ thể.
2H + - 2e - → H2 (tại điện cực Pt) Phương trình tổng quát:
Quá trình sản xuất hydro quang xúc tác và lọc nước/không khí dựa vào các phản ứng khử và oxy hóa Sử dụng chất bán dẫn nano có thể tăng cường hiệu quả của các phản ứng hấp phụ bề mặt và quang xúc tác nhờ vào diện tích bề mặt phản ứng lớn hơn Để sản xuất hydro, mức vùng dẫn cần âm hơn mức tạo hydro (EH2/H2O), trong khi vùng hóa trị phải dương hơn mức oxy hóa của nước (EO2/H2O) để đảm bảo sản xuất oxy hiệu quả từ nước Với hoạt tính xúc tác mạnh và độ ổn định hóa học cao, quá trình này có khả năng tránh được nhiều vấn đề liên quan đến hiệu suất.
LÝ THUYẾT VỀ NGUYÊN TỐ ĐẤT HIẾM
1.2.1 Tổng quan về các nguyên tố đất hiếm
Các nguyên tố đất hiếm bao gồm họ Lanthan với 15 nguyên tố từ Lantan (La) đến Luteti (Lu), cùng với hai nguyên tố Scandium (Sc) và Yttrium (Y) Yttrium và Scandium thường xuất hiện trong cùng lớp trầm tích với họ Lanthan và có những tính chất hóa học tương đồng.
Do đó chúng cũng được xem là đất hiếm Cấu hình điện tử của đất hiếm được đưa ra trong bảng 1.4
Bảng 1.4 Cấu trúc điện tử và trạng thái cơ bản của các ion RE 3+
Theo thuyết cấu tạo hóa học, cấu trúc lớp điện tử trong nguyên tử các nguyên tố đất hiếm hình thành khi lớp điện tử S của lớp thứ sáu (6s²) được bão hòa bằng hai điện tử, sau đó lớp điện tử 4f được lấp đầy dần với 14 điện tử Do sự khác biệt trong cấu trúc lớp vỏ điện tử 4f, các nguyên tố này có những tính chất vật lý khác nhau, đặc biệt là về tính chất quang.
Eu 3+ phát ánh sáng đỏ, Sm 3+ phát ánh sáng cam, Tb 3+ phát ánh sáng xanh lá cây,
Ion Tm 3+ phát ra ánh sáng xanh dương nhờ vào cấu trúc phân lớp điện tử của nó Các ion này có phân lớp 4f được bảo vệ bởi hai phân lớp bên ngoài là 5s và 5p, giúp giảm thiểu sự nhiễu loạn từ môi trường xung quanh Sự bảo vệ này cho phép các điện tử quang học trong phân lớp 4f ít bị ảnh hưởng bởi trường tinh thể, điều này được minh họa trong hình 1.8.
Nhà vật lý học Dieke và nhóm nghiên cứu đã khảo sát chính xác các mức năng lượng của điện tử 4f cho 13 nguyên tố đất hiếm, với giản đồ năng lượng từ trạng thái cơ bản đến các trạng thái kích thích được mô tả theo thang năng lượng (cm -1) Hình ảnh minh họa cấu trúc của nguyên tử ion Re 3+ và kim loại chuyển tiếp, được gọi là giản đồ Dieke, thể hiện rõ ràng các mức năng lượng này.
Hình1.9 Giản đồ cấu trúc mức năng lượng Dieke
1.2.2 Sự chuyển dịch mức năng lượng của ion đất hiếm Đối với đất hiếm, 2 orbital khác nhau tham gia vào quá trình chuyển dịch điện tử:
Orbital 4f chứa các electron không bắt cặp, đóng vai trò quan trọng trong việc tạo ra các tính chất điện và từ của đất hiếm Những orbital này được bảo vệ bởi các orbital có bán kính lớn hơn như 5s và 5d Tính chất quang liên quan đến chuyển dịch 4f - 4f hoàn toàn độc lập với mạng nền.
Orbital 5d nằm cao hơn mức 4f về mặt năng lượng và chịu ảnh hưởng mạnh mẽ từ trường tinh thể cũng như tính đối xứng của mạng nền Đối với ion Ce 3+ và Eu 2+, các orbital này có mức năng lượng thấp, dẫn đến hiện tượng phát quang trong vùng nhìn thấy thông qua quá trình hấp thụ 4f-5d và phát xạ 5d-4f Nhờ vào tính nhạy cảm của chúng với bản chất hóa học của mạng nền, nhiều màu sắc phát xạ đa dạng có thể được tạo ra.
Ví dụ, Eu 2+ có thể phát xạ màu xanh dương trong nhôm hydoxit, nhưng phát xạ màu đỏ trong sulphit SrS [13]
Các dịch chuyển điện từ trong vật liệu pha tạp đất hiếm được phân loại như sau:
- Dịch chuyển điện từ trong cấu hình 4f: 4f-4f
- Dịch chuyển điện tử giữa cấu hình 4f và 5d (4f5d): 4f n → 4f n-1 -5d 1
Chuyển đổi điện tích (CT) giữa các mức 4f và phối tử (L) diễn ra theo quá trình 4f n -L→4f n+1 -L n-1 Bản chất và cường độ của dịch chuyển điện tử giữa các mức năng lượng được giải thích bởi sự tương tác giữa trường điện từ và vật liệu, dẫn đến nhiều dịch chuyển cho phép hoặc bị cấm, bao gồm lưỡng cực điện (ED), lưỡng cực từ (MD) và tứ cực điện (EQ).
Theo quy tắc lựa chọn Laporte, dịch chuyển ED chỉ xảy ra khi các orbital có tính đối xứng khác nhau, như 4f-5d, và dịch chuyển CT Ngược lại, dịch chuyển ED bị cấm với 4f-4f, trong khi dịch chuyển MD được cho phép Quy tắc này áp dụng cho electron tự do, nhưng có thể không còn đúng trong vật liệu do tác động của mạng nền Khi ion đất hiếm ở vị trí không đối xứng, sự trộn lẫn giữa orbital 4f và 5d do trường tinh thể gây ra cho phép dịch chuyển ED, được gọi là “cảm ứng” hay “cưỡng bức” Điều này đặc biệt rõ ràng trong vật liệu phát quang pha tạp ion Eu 3+ Trong mọi trường hợp, tương tác lưỡng cực điện luôn có cường độ lớn hơn hẳn so với MD (ED >> MD), như thể hiện qua sự tách mức năng lượng của ion Eu 3+.
Các đặc trưng chính của chuyển dịch 4f-4f được trình bày như sau:
Các đỉnh phát xạ nhọn được tạo ra bởi trường tinh thể của mạng nền, mà không có tác động động học Điều này có nghĩa là sự tương tác với các phonon (dao động mạng) là rất yếu.
Năng lượng của dịch chuyển đặc trưng 4f-4f trong các nguyên tố đất hiếm là giống nhau, tuy nhiên cường độ của chúng có sự thay đổi Nguyên nhân chính là do tác động của trường tinh thể từ mạng nền lên các mức năng lượng trong cấu hình 4f là rất nhỏ.
- Cường độ phát xạ thấp, vì theo quy tắc lựa chọn, dịch chuyển ED bị cấm
Do sự hiện diện của nhiều mức năng lượng trong cấu hình 4f, hầu hết các nguyên tố đất hiếm đều cho thấy sự dịch chuyển điện tử đáng kể, dẫn đến chất lượng màu sắc thấp Điều này được coi là một hạn chế trong các ứng dụng thực tiễn.
Các đặc trưng của dịch chuyển 4f-5d được trình bày như sau:
- Phổ hấp thụ - phát xạ của các dịch chuyển 4f-5d/5d-4f luôn gồm 1 dải rộng Tác động của của trường tinh thể lên orbital 5d lớn Sự bắt cặp với phonon cao
- Năng lượng (bước sóng) của dịch chuyển 4f-5d phụ thuộc vào bản chất hóa học của mạng nền
- Cường độ phát xạ cao ( dịch chuyển ED cho phép)
Đối với hầu hết các loại đất hiếm, sự dịch chuyển 4f-5d thường có năng lượng quá cao để có thể ứng dụng thực tế Tuy nhiên, trong các ion RE 3+, chỉ có Ce 3+, Tb 3+ và Pr 3+ có sự dịch chuyển 4f-5d không quá xa vùng khả kiếm, nằm trong khoảng 200nm.
1.2.3 Đặc trưng quang phổ của các nguyên tố đất hiếm
- Quang phổ của nguyên tố Europium (Eu)
Mức kích thích thấp nhất (5D0) của ion Eu 3+ là mức đơn không suy biến (J0), với các chuyển tiếp trường tinh thể 5D0 → 7F1 và 5D0 → 7F2 Sau khi hấp thụ UV dưới 400 nm, phổ phát xạ tại nhiệt độ phòng cho thấy các phát xạ từ các chuyển tiếp 5D0 → 7FJ (J = 0–4) có tâm tương ứng ở khoảng 580, 593, 613, 653 và 702 nm Ngoài ra, một phát xạ nhỏ ở bước sóng 540 nm được quan sát là từ mức 5D1 được kích thích cao hơn, với vị trí và cường độ tương đối của phát xạ phù hợp với dữ liệu tài liệu trước đó.
Hình 1.10 Phổ phát xạ của ion Eu 3+
- Đặc trưng quang phổ của nguyên tố Erbium (Er)
Ion Er 3+ trong TiO2 có khả năng hấp thụ trong dải quang phổ từ UV đến 800 nm, và khi kết hợp với ion Yb 3+, khả năng hấp thụ mở rộng đến 1200 nm Để xác định sự phát xạ trong khoảng 520–700 nm, bước sóng kích thích 488 nm được sử dụng, với phổ phát xạ được minh họa trong hình 1.11 Sự kết hợp của quá trình chuyển đổi 2H11/2 → 4I15/2 và 4S3/2 → 4I15/2 cho thấy sự phát xạ rộng trong dải 540–575 nm.
Hình 1.11 Phổ phát xạ của ion Er 3+
- Đặc trưng quang phổ của nguyên tố Thulium (Tm)
Sự hấp thụ của ion thulium trong mẫu cho thấy sự hấp thụ nhỏ ở bước sóng
Bước sóng 470 nm được sử dụng để kích thích trực tiếp ion Tm3+, với sự hấp thụ mạnh hơn ở các bước sóng 690, 795 và 1210 nm Phổ phát xạ trong khoảng 490–780 nm cho thấy đỉnh cực đại tại 495 nm, xuất phát từ quá trình chuyển đổi 1G4 → 5H6 Ngoài ra, cường độ rất thấp của nhóm vạch trong khoảng 650–670 nm có thể liên quan đến quá trình chuyển đổi 1G4 → 3F4.
Hình 1.12 Phổ phát xạ của ion Tm 3+
MỘT SỐ PHƯƠNG PHÁP CHẾ TẠO VẬT LIỆU TIO 2 NANO
Trong ngành công nghệ vật liệu, sol-gel đã có lịch sử khoảng 30 năm, bắt đầu từ việc chế tạo gốm thủy tinh và gốm sứ Quy trình tổng hợp sol-gel đơn giản, thao tác dễ dàng, mang lại độ đồng đều cao và đảm bảo độ tinh khiết của vật liệu Công nghệ này cho phép tổng hợp TiO2 nano dưới nhiều dạng khác nhau như bột, hạt, màng và dạng khối.
Phương pháp sol-gel bắt đầu từ dung dịch tiền chất, bao gồm hợp chất kim loại muối halogen, nước, rượu và axit hoặc bazơ làm xúc tác Qua các phản ứng thủy phân và đa trùng ngưng, các hợp chất kim loại tạo thành sol chứa polyme hoặc hạt nhỏ phân tán Các phản ứng này tiếp tục làm tăng kích thước và kết nối các hạt cho đến khi sol chuyển thành gel ướt, bao gồm khung oxit kim loại trong môi trường lỏng Sau khi ủ và sấy gel ướt để loại bỏ dung môi và nước, chúng ta thu được gel khô hay xerogel Cuối cùng, nung gel ở nhiệt độ cao hơn sẽ tạo ra gel nung với cấu trúc chặt hơn.
Trong quá trình chế tạo vật liệu nano TiO2, phản ứng thủy phân diễn ra khi nước được thêm vào, dẫn đến việc thay thế các gốc alkoxide liên kết với Ti(IV) bằng các gốc hydroxyl (OH) Đồng thời, phản ứng trùng ngưng xảy ra, biến đổi các liên kết Ti – O, tạo ra cấu trúc vật liệu nano ổn định hơn.
OH thành các liên kết Ti – O – Ti, sản phẩm phụ là nước và rượu
Bảng 1.5 Tổng hợp điều kiện thực nghiệm và tính chất hình thái của nano TiO2 sản xuất bằng phương pháp sol – gel [3]
Nhiệt độ và thời gian nung
Kích thước tinh thể (nm)
Tỉ lệ pha và hình thái
Phương pháp thủy nhiệt được thực hiện trong nồi hấp bằng thép áp suất cao, có thể có hoặc không có lớp lót Teflon Phản ứng diễn ra dưới điều kiện nhiệt độ và áp suất cao, giúp tăng cường độ hòa tan và tốc độ phản ứng giữa các chất Quy trình này bao gồm nhiều giai đoạn khác nhau.
- Sư nung kết thủy nhiệt
- Sự phân hủy thủy nhiệt
- Quá trình ổn định cấu trúc vật liệu
Trong quá trình sản xuất tinh thể nano, việc điều chỉnh các thông số như áp suất nước, nhiệt độ, thời gian xử lý và hệ thống tiền chất là rất quan trọng để duy trì tỷ lệ tạo mầm cao và phân bố kích thước thích hợp Phương pháp xử lý thủy nhiệt nổi bật với khả năng điều chế hạt TiO2 có kích thước và hình dạng mong muốn, đồng thời đảm bảo tính đồng nhất về thành phần và độ kết tinh cao ở nhiệt độ thấp Kỹ thuật này giúp giảm sự kết tụ giữa các hạt, tạo ra phân bố kích thước hạt hẹp, đồng nhất pha và kiểm soát hình thái hạt Ngoài ra, phương pháp này còn cung cấp thành phần đồng nhất, độ tinh khiết cao của sản phẩm, cũng như kiểm soát hiệu quả hình dạng và kích thước của các hạt.
Bảng 1.6 Tổng hợp điều kiện thí nghiệm và tính chất hình thái của nano TiO2 sản xuất bằng phương pháp thủy nhiệt [3]
Nhiệt độ và thời gian Kích thước tinh thể
Tỉ lệ pha và hình thái
Hình xốp và sợi A: Anatase
TBO: Titanium (IV) butoxide (Ti(OCH2CH2CH3)4)
TBOT: Tetrabutyl orthotitanate (Ti(OCH4H9)4)
Ngoài hai phương pháp phổ biến đã đề cập, còn có nhiều kỹ thuật khác để chế tạo vật liệu nano TiO2, bao gồm phương pháp lắng đọng hơi hóa học, phương pháp điện hóa, phương pháp Micelle và Micelle nghịch đảo, cũng như phản ứng hóa học hỗ trợ bởi sóng siêu âm.
THỰC NGHIỆM VÀ PHƯƠNG PHÁP PHÂN TÍCH
HÓA CHẤT VÀ THIẾT BỊ
Quá trình chế tạo vật liệu TiO2 và TiO2 pha tạp đất hiếm yêu cầu sử dụng các hóa chất được liệt kê trong bảng 2.1 Các hóa chất này được sử dụng trực tiếp trong thí nghiệm mà không cần tinh chế và được bảo quản tại phòng thí nghiệm hóa thuộc bộ môn Vật lý chất rắn, Khoa Vật lý – Vật lý kỹ thuật, Đại Học Khoa Học Tự Nhiên, ĐHQG Thành phố Hồ Chí Minh.
Bảng 2.1 Danh sách hóa chất sử dụng Tên hóa chất Công thức Độ tinh khiết Tetraisopropyl orthotitanate - TTIP
RE (III) nitrat RE: Eu, Er, Tm
Trong quá trình sản xuất vật liệu TiO2 pha tạp đất hiếm, các thiết bị cần thiết được cung cấp bởi bộ môn Vật lý chất rắn, Trường Đại học Khoa học Tự Nhiên, ĐHQG TP Hồ Chí Minh Danh sách các thiết bị này được trình bày chi tiết trong bảng 2.2.
Bảng 2.2 Danh sách thiết bị được sử dụng
Tên thiết bị Công dụng Hình ảnh
Máy siêu âm Vệ sinh dụng cụ thí nghiệm, giúp hòa tan muối vào dung dịch
Lò sấy chân không Sấy khô các dụng cụ thí nghiệm
Máy khuấy từ Khuấy đều hóa chất trong cốc, làm tăng tốc độ phản ứng
Cân tiểu ly Cân hóa chất chính xác với độ chia nhỏ nhất 1mg
Lò nung Nung mẫu ở nhiệt độ cao
Trong thí nghiệm này, ngoài các thiết bị chính, tôi còn sử dụng nhiều dụng cụ trong phòng thí nghiệm như ống nghiệm, ống đong, cốc thủy tinh, chai lọ thủy tinh, cuvet nhựa và cá từ để đảm bảo tính chính xác và hiệu quả của thí nghiệm.
QUY TRÌNH THỰC NGHIỆM
- Bước 1: Làm sạch các dụng cụ thí nghiệm
Bước 2: Đong thể tích các chất gồm tetraisopropyl orthotitanate (TTIP) 14,7 ml, ethanol 58 ml, axit nitric 0,26 ml và nước cất 2,7 ml Đồng thời, cân khối lượng của các hợp chất Eu(NO3)3.5H2O, Er(NO3)3.5H2O, Tm(NO3)3.5H2O lần lượt là 0,0445g, 0,0443g và 0,0445g.
- Bước 3: Cho từ từ TTIP vào dung dịch ethanol đang đặt trên máy khuấy từ Sau đó tiếp tục khuấy trong 30 phút
Bước 4: Từ từ thêm hỗn hợp dung dịch axit nitric và nước cất (cùng với RE(NO3)3.5H2O nếu cần chế tạo mẫu pha tạp) vào hỗn hợp đã chuẩn bị, sau đó khuấy đều trong 60 phút.
- Bước 5: Sau khi quá trình gel hóa hoàn tất, sấy mẫu ở 120◦C trong 2h (mẫu chuyển sang màu vàng)
- Bước 6: Nung mẫu ở từng nhiệt độ khác nhau (600◦C, 700◦C, 800◦C, 900◦C), trong 1h
- Bước 7: Để mẫu hạ nhiệt xuống nhiệt độ phòng và bắt đầu các phương pháp phân tích
Sơ đồ 2.1 Quy trình chế tạo hạt nano TiO2 và TiO2 pha tạp
H2O + HNO3 [+ RE(NO3)3.5H2O] Khuấy từ 30 phút
Thu TiO2 (hoặc TiO2:RE)
MỘT SỐ PHƯƠNG PHÁP PHÂN TÍCH
Nhiễu xạ tia X là hiện tượng xảy ra khi các chùm tia X tương tác với các mặt tinh thể của chất rắn, nhờ vào cấu trúc tinh thể tuần hoàn tạo ra các cực đại và cực tiểu nhiễu xạ Giản đồ nhiễu xạ thể hiện mối quan hệ giữa cường độ nhiễu xạ và 2 lần góc nhiễu xạ (2θ).
Hình 2.1 Máy nhiễu xạ tia X Dựa vào phương pháp nhiễu xạ tia X, ta có thể tính được kích thước hạt bằng phương trình Scherrer
K là hằng số không thứ nguyên λ là bước sóng của bức xạ tia X
2θ là nhiễu xạ góc β là chiều rộng đầy đủ ở nửa cực đại (FWHM) của nhiễu xạ đỉnh
Tỉ lệ pha anatase, ký hiệu XA, trong vật liệu được xác định thông qua phương trình liên quan đến cường độ đỉnh anatase (101) tại góc nhiễu xạ 2θ là 25,3° và cường độ đỉnh rutile (110) tại góc nhiễu xạ 2θ là 27,4°.
2.3.2 Phương pháp phổ hấp thụ khả kiến (UV-vis)
Khi chiếu sáng với bước sóng phù hợp qua dung dịch chất màu, các phân tử trong dung dịch sẽ hấp thụ một phần năng lượng của chùm sáng, trong khi phần còn lại sẽ truyền qua Bằng cách xác định cường độ ánh sáng truyền qua, chúng ta có thể tính toán nồng độ của dung dịch Hiện tượng hấp thụ ánh sáng trong dung dịch tuân theo định luật Bughe – Lambert – Beer.
A = ε l C ε là độ hấp thụ quang riêng, với giá trị là hằng số khác nhau với từng chất l là độ dày truyền quang (cm)
C là nồng độ mẫu (mol/l)
Hình 2.2 Thiết bị đo phổ Uv-vis
2.3.3 Phương pháp phổ hấp thụ hồng ngoại FT – IR
Khi được chiếu sáng, các liên kết hóa học trong vật liệu hấp thụ bước sóng hồng ngoại một cách có chọn lọc và dao động với các vận tốc khác nhau Phổ dao động này được gọi là phổ hấp thụ hồng ngoại (FT-IR), cung cấp thông tin nhanh chóng và chính xác về cấu trúc phân tử mà không cần sử dụng các phương pháp tính toán phức tạp.
Hình 2.3 Thiết bị đo phổ FT – IR
2.3.4 Phương pháp phổ tán xạ Raman
Trong quang phổ Raman, mẫu được chiếu sáng bằng chùm laser mạnh trong vùng tử ngoại – khả kiến (v0), và ánh sáng tán xạ thường được quan sát theo phương vuông góc với chùm tia tới Ánh sáng tán xạ bao gồm hai loại: chùm tia Rayleigh, mạnh và có tần số giống với tia tới (v0), và tán xạ Raman, yếu hơn (~10^-15 lần chùm tia tới) với tần số là v0 ± vm, trong đó vm là tần số dao động phân tử Vạch v0 - vm được gọi là vạch Stokes.
Trong quang phổ Raman, tần số dao động (vm) được đo dựa trên sự dịch chuyển so với tần số chùm tia tới (v0) Khác với phổ hồng ngoại, phổ Raman được thực hiện trong vùng tử ngoại – khả kiến, nơi mà các vạch kích thích (laser) và các vạch Raman xuất hiện đồng thời.
Phương pháp phổ Raman có những ưu điểm sau:
- Không tiếp xúc với mẫu và không phá hủy chúng
- Chỉ cần một lượng nhỏ mẫu và không cần chuẩn bị mẫu trước
- Có thể áp dụng cho chất rắn, lỏng, dung dịch và một vài chất khí
- Phân tích tương đối nhanh và cho kết quả chính xác
2.3.5 Phương pháp phổ phát quang
Phổ phát quang biểu diễn sự phụ thuộc của cường độ phát quang (IPL) theo bước sóng ứng với một bước xạ kích thích
Phổ phát quang (PL) là công cụ quan trọng để thu thập thông tin về cấu trúc điện tử của các ion phát quang như Er3+, Eu3+ và Tm3+ Nó cũng giúp phân tích quá trình truyền năng lượng giữa các tâm phát quang khác nhau và cung cấp dữ liệu về năng lượng vùng cấm.
Bán dẫn có sự phụ thuộc nhiệt độ rõ rệt, trong đó phổ phát quang thể hiện mối quan hệ giữa cường độ ánh sáng phát quang (IPL) và bước sóng dưới tác động của bức xạ kích thích cụ thể Hình dạng của phổ bức xạ phản ánh sự chuyển đổi giữa các mức năng lượng điện tử, có thể xuất hiện dưới dạng các vạch hẹp hoặc dải rộng, tùy thuộc vào tâm quang học và trường tinh thể.
1 Hình 2.4 Cấu tạo hệ đo phổ quang phát quang
1: Nguồn kích thích đơn sắc 7: Máy đơn sắc bức xạ
2,4: Hệ thống thấu kính hội tụ 8: Nhân quang điện
3: Giá mẫu 9: Bộ khuếch đại
5: Bộ điều biến 10: Máy tính
2.3.6 Kính hiển vi điện tử quét SEM
Kính hiển vi điện tử quét (SEM) là thiết bị tạo ra hình ảnh có độ phân giải cao bằng cách sử dụng chùm điện tử quét trên bề mặt mẫu vật Khi chùm điện tử tương tác với bề mặt, các bức xạ như điện tử thứ cấp và điện tử tán xạ ngược sẽ được phát ra Quá trình tạo ảnh và phân tích trong SEM dựa trên việc phân tích các bức xạ này, từ đó cung cấp thông tin chi tiết về cấu trúc và tính chất của mẫu vật.
- Đối với điện tử thứ cấp: thu được ảnh hai chiều của bề mặt mẫu
- Đối với điện tử tán xạ ngược: thu được thành phần hóa học ở bề mặt mẫu, cấu trúc tinh thể, thông tin về các domain sắt điện,…
Thiết bị SEM, mặc dù không đạt độ phân giải cao như TEM, lại có ưu điểm nổi bật là khả năng phân tích mẫu mà không cần phá hủy Điều này, kết hợp với các thao tác điều khiển đơn giản, giúp người dùng dễ dàng sử dụng hơn Hơn nữa, chi phí đầu tư cho SEM cũng thấp hơn so với TEM, làm cho nó trở thành lựa chọn hợp lý cho nhiều ứng dụng.
Hình 2.6 Thiết bị đo SEM
VÀ VẬT LIỆU NANO PHA TẠP RE
Kích thích bằng tia UV
Phổ hấp thụ của MB trong khoảng 450 – 725 nm được khảo sát, cho thấy sự thay đổi cường độ theo thời gian chiếu đèn Các hình 3.10.a, 3.11.a, 3.12.a, và 3.13.a minh họa sự giảm nhẹ của các đỉnh cường độ sau thời gian chiếu đèn từ 0 phút đến 120 phút.
Hình 3.10.a) Phổ hấp thụ và b) khả năng phân hủy chất màu MB của TiO2 dưới kích thích tia UV a) b)
Hình 3.11.a) Phổ hấp thụ và b) khả năng phân hủy chất màu MB của TiO2:Eu dưới kích thích tia UV
Hình 3.12.a) Phổ hấp thụ và b) khả năng phân hủy chất màu MB của TiO2:Er dưới kích thích tia UV
Hình 3.13.a) cho thấy phổ hấp thụ và b) khả năng phân hủy chất màu MB của TiO2:Tm dưới kích thích tia UV Qua các phổ UV-Vis ở hình 3.10a, 3.11a, 3.12a, và 3.13a, nhận thấy rằng vật liệu TiO2 pha tạp có độ hấp thụ MB không đáng kể, trong khi TiO2 thuần hấp thụ mạnh trong 15 phút đầu của quá trình kích thích Để làm rõ sự thay đổi cường độ phổ hấp thụ, chúng tôi đã tích phân cường độ của tất cả các phổ hấp thụ theo từng mẫu và vẽ theo thời gian chiếu đèn Hình 3.14 cho thấy kết quả của 3 mẫu pha tạp.
Nghiên cứu cho thấy rằng nồng độ MB của TiO2 thuần giảm mạnh khi được chiếu tia UV, tuy nhiên không có sự khác biệt rõ ràng trong tính chất xúc tác quang dưới tác động của tia UV giữa ba loại TiO2 pha tạp được chế tạo.
Hình 3.14 trình bày quá trình phân hủy chất màu MB dưới tác động của tia UV, sử dụng TiO2 thuần và TiO2 pha tạp Bảng so sánh hiệu suất phân hủy của bốn loại mẫu khác nhau cho thấy sự khác biệt rõ rệt trong khả năng xử lý chất màu này.
Bảng 3.4 So sánh hiệu suất phân tủy MB của TiO2 thuầnvà TiO2 pha tạp với kích thích tia UV
Hiệu suất phân hủy MB trong
Phân hủy MB do hấp phụ (60 phút đầu)
Phân hủy MB do hấp thụ (120 phút sau)
Kết quả từ bảng 3.4 cho thấy hiệu suất phân hủy chất màu MB của TiO2 và TiO2 pha tạp RE đều cao, đạt trên 70%, ngoại trừ mẫu TiO2 pha tạp Er Hiệu suất phân hủy khác nhau tùy thuộc vào loại pha tạp, với mẫu TiO2 có hiệu suất cao nhất đạt 94,63%, trong khi mẫu TiO2:Er có hiệu suất thấp nhất chỉ đạt 53,71%.
TiO2:Tm có hiệu suất phân hủy do hấp phụ khi chưa chiếu sáng là lớn nhất
85,35% và TiO2 có hiệu suất phân hủy cho hấp thụ dưới điều kiện chiếu tia UV là lớn nhất (48,63%)
Kích thích bằng bước sóng λ = 980 nm
Chúng tôi đã thực hiện khảo sát khả năng quang xúc tác của mẫu không chỉ dưới kích thích tia UV mà còn dưới ánh sáng với bước sóng λ.
= 980 nm Dưới đây là phổ hấp thụ và tỉ lệ phân hủy MB của TiO2 thuần và TiO2 pha tạp
Hình 3.15.a) Phổ hấp thụ và b) khả năng phân hủy chất màu MB của TiO2 dưới kích thích λ = 980 nm
Hình 3.16.a) Phổ hấp thụ và b) khả năng phân hủy chất màu MB của TiO2:Eu dưới kích thích λ = 980 nm
Hình 3.17.a) Phổ hấp thụ và b) khả năng phân hủy chất màu MB của TiO2:Er dưới kích thích λ = 980 nm a) a) a) b) b) b)
Hình 3.18.a) Phổ hấp thụ và b) khả năng phân hủy chất màu MB của TiO2:Tm dưới kích thích λ = 980 nm
Các mẫu chứa TiO2 thuần và TiO2 pha tạp cho thấy độ hấp thụ giảm dần theo thời gian, trong đó các mẫu pha tạp có độ hấp phụ mạnh hơn so với mẫu TiO2 thuần Qua việc tích phân cường độ của các phổ hấp thụ theo từng mẫu và vẽ theo thời gian chiếu đèn, mặc dù nồng độ chất màu MB không suy giảm nhiều, nhưng TiO2:Er lại cho thấy hiệu quả hấp phụ tốt nhất.
Hình 3.19 Độ phân hủy MB dưới dưới kích thích λ = 980 nm của TiO2 thuần và
TiO2 pha tạp Bảng 3.5 So sánh hiệu suất phân tủy MB của TiO2 thuần và TiO2 pha tạp dưới kích thích λ = 980 nm λ = 980 nm
Hiệu suất phân hủy MB trong
Phân hủy MB do hấp phụ (60 phút đầu)
Phân hủy MB do hấp thụ (120 phút sau)
Theo bảng 3.5, trong khoảng thời gian từ -60 phút đến 0 phút, mẫu TiO2:Er đạt độ phân hủy MB cao nhất với 62,89% nhờ vào khả năng hấp phụ Trong khi đó, từ 0 phút đến 120 phút, mẫu TiO2:Eu cho thấy độ phân hủy MB cao nhất là 11,58% nhờ vào quá trình hấp thụ dưới tác động của bước sóng λ = 980 nm.
So sánh hiệu suất phân hủy MB giữa hai điều kiện kích thích khác nhau trong bảng 3.4 và 3.5 cho thấy rằng mẫu TiO2 thuần có hiệu ứng quang xúc tác mạnh nhất khi kích thích bằng tia UV, trong khi mẫu TiO2 pha tạp Er lại thể hiện hiệu ứng quang xúc tác mạnh nhất dưới điều kiện kích thích tia hồng ngoại.
Trong khóa luận này, chúng tôi nghiên cứu chế tạo và khảo sát tính quang của vật liệu nano TiO2 pha tạp đất hiếm Eu 3+, Er 3+ và Tm 3+ Các vật liệu chế tạo đạt được cấu trúc và hình thái mong muốn, mở ra tiềm năng ứng dụng cao trong thực tiễn, bao gồm sản xuất vật liệu tự làm sạch và các thiết bị linh kiện điện tử.
1 Chúng tôi đã chế tạo thành công vật liệu TiO2 và vật liệu TiO2 pha tạp đất hiếm bằng phương pháp sol – gel Khảo sát được hình dạng và cấu trúc của hạt nano TiO2 thuần và TiO2 pha tạp Khảo sát được kích thước trung bình của hạt nano TiO2 pha tạp Er là 22 nm
2 Phổ phát xạ huỳnh quang của các mẫu được kích thích ở bước sóng
325 nm cho các chuyển dời với bước xạ màu xanh lá 4 S3/2 – 4 I15/2 tại bước sóng
565 nm và đỏ 4 F9/2 tại bước sóng 667 nm
3 Khảo sát hiệu ứng quang hóa phân hủy MB của hạt nano TiO2 thuần và TiO2 pha tạp dưới đèn UV và đèn hồng ngoại, thì thu được hiệu ứng quang hóa phân hủy MB Dưới kích thích đèn UV thì mẫu TiO2 là tốt nhất, còn dưới kích thích của đèn hồng ngoại thì mẫu TiO2 pha tạp Er là tốt nhất
KIẾN NGHỊ VÀ ĐỊNH HƯỚNG PHÁT TRIỂN
Do thời gian nghiên cứu có hạn, chúng tôi chưa thể tìm hiểu sâu về cấu trúc, tính chất quang học và ứng dụng của vật liệu TiO2 pha tạp đất hiếm Các hướng nghiên cứu tiếp theo sẽ tập trung vào việc khám phá những khía cạnh này một cách chi tiết hơn.
1 Thực hiện thêm một số phép đo nhằm phân tích và tính toán các vị trí có thể có của các ion Re 3+ trong mạng nền vật liệu TiO2, sự ảnh hưởng của vị trí của nó đến cấu trúc và tính chất quang của vật liệu
2 Tiếp cận với một số phương pháp khác đồng thời thay đổi một vài thông số như nhiệt độ, độ pH, thời gian, tiền chất để chế tạo vật liệu TiO2 với những dạng thù hình khác nhau (hình cầu, hình dây, hình bông hoa, hình bông súp lơ) và ứng dụng vào chế tạo cảm biến khí
3 Thay đổi nồng độ pha tạp và ứng dụng vào việc chế tạo các thiết bị linh kiện điện huỳnh quang, các thiết bị thông tin quang
4 Khảo sát hiệu ứng quang xúc tác thông qua làm mất màu dung dịch
MB của vật liệu TiO2 được pha tạp với nhiều loại nguyên tố khác nhau và đồng pha tạp, dưới nhiều điều kiện chiếu xạ như ánh sáng hỗn hợp và ánh sáng tự nhiên, nhằm ứng dụng vào các vật liệu tự làm sạch.